福布斯:2015年成為66年來藥物獲批最多的一年
過去幾年來,制藥界尤其是生物制藥領域的發展速度令人咋舌。福布斯(Forbes)網站最近對2015年獲批新藥進行的回顧統計,也印證了這個趨勢。
2015年對于醫藥創新是非同尋常的一年。這一年已經發生的事情在幾年前都只能說是夢(或者干脆說是幻想):去年的新藥審批數量達到了51個,比1950年以來的任何一年都多。這些藥物包括被FDA的藥品審評中心(CDER)批準的45種藥物注1,和生物制品評價和研究中心(CBER)批準的6種重組療法注2。后者包括治療血液凝固病癥(例如,血友病)的四種藥物,以及治療黑素瘤疫苗和針對B型球菌性腦膜炎的預防性疫苗。
群雄爭霸?
這51種藥物來自于39家公司,其中有8家公司有不止一種藥物獲得批準。這些巨頭中,無可爭議的冠軍是諾華(Novartis),拿到了5個藥物批準;其次是安進(Amgen),將3個批準收入囊中。其它的領先者是阿特維斯(Actavis)、Alexion、Baxalta、百時美施貴寶(Bristol-Myers Squibb)、強生(Johnson & Johnson)和羅氏(Roche),每家都有兩個批準。如果我們回顧過去五年和十年的審批情況,會發現一些有趣的趨勢:
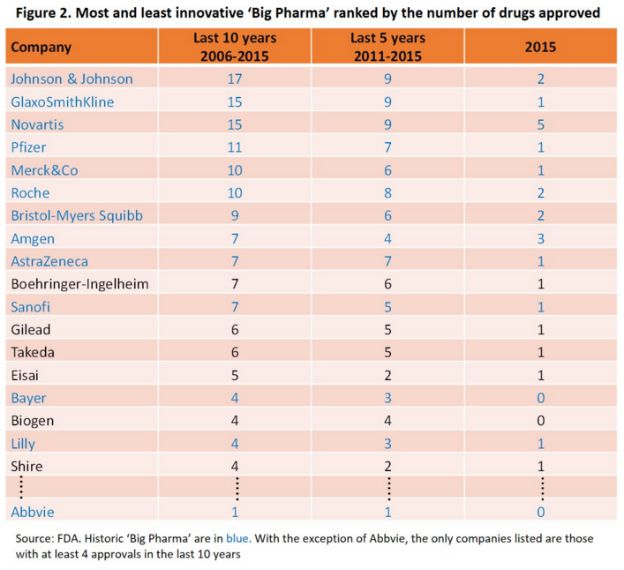
(1)前三位的企業都是一樣的:強生、葛蘭素史克(GSK)和諾華。
(2)最后三位的大型藥企(Big Pharma,上圖中藍色字體)也一樣:拜耳(Bayer)、禮來(Lilly)和艾伯維(Abbvie)。
(3)在過去十年中,排名前三的制藥企業巨頭總共已經為市場帶來了47種藥品,而排名末尾的三個藥企的藥物產品還不到10種。
(4)傳統上一直被視為“中等規模”的少數幾家公司也擠進了前列,這也許預示著行業領導者的重新洗牌,并使業界人士重新審視獲得“藥界大佬”資格的標準。
生物藥物和首創藥物創出新高
這些被批準的藥物中,有39%的藥物(20種)屬于生物藥物,這一比例比2014年的35%和2013年的22%都有所上升,這證實了在醫藥工業研發管道中生物制藥的重要性日益增加。另外有39%的藥物(20種)屬于功能上的首創藥物(first-in-class),這與2014年的39%和2013年的37%基本一樣。這種依賴于FDA統計的劃分方式似乎有點保守,也有人認為下面的藥物也應列入首創性藥物行列:
Farydak:治療多發性骨髓瘤的第一種HDAC抑制劑
Unituxin:僅有的獲得批準的神經節苷脂GD2的抑制劑
Kybella:第一種針對頦下脂肪(雙下巴)的藥物
Natpara:可激活甲狀旁腺激素2受體,它與Forteo不同,后者通過結合到甲狀旁腺激素/甲狀旁腺激素相關肽受體而起作用。
如果把這些藥物加入首創藥物,則首創藥物所占比例將躍升為47%,這相對于幾年前整個藥物行業被抨擊為“吃老本”的狀況是個顯著的好轉。
腫瘤藥物突飛猛進,神經藥物遲滯落后
四個藥物治療領域占了所有批準藥物的63%。其中癌癥領域有16個新藥獲批,這比該領域去年的8個批準翻了一倍,而且也占據了2015年全部批準的最大一塊份額,幾乎達到三分之一。
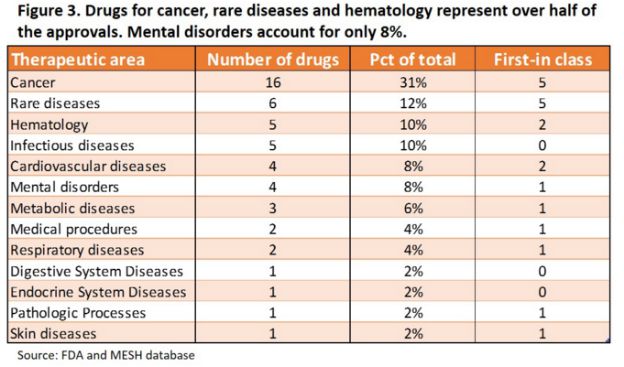
治療傳染病的藥物有5種,雖然低于去年的12種,但還是包括了疫苗、抗細菌藥、抗真菌藥和抗病毒藥等多種藥物。
血液病藥物再次表現強勁,獲得5種藥物的批準,使治療血液病(主要是血友病)的新療法在過去的五年中達到了13種,這與之前20年里的批準總量相當。
不過也有不那么積極的一面,精神疾病的新治療方法與2014年一樣疲軟,只有4個批準。

分享到:










 相關新聞
相關新聞