- 近年來(lái),抗體類藥物(如單抗、雙抗、ADC等)發(fā)展迅速,在多個(gè)疾病研究領(lǐng)域均有重磅產(chǎn)品陸續(xù)上市,抗體藥物研發(fā)受到越來(lái)越多的關(guān)注。美迪西在抗體藥物的一站式研發(fā)服務(wù)方案制定中與客戶深入交流,將每一個(gè)案例的特點(diǎn)與多年實(shí)戰(zhàn)經(jīng)驗(yàn)和技術(shù)積累相結(jié)合,謹(jǐn)慎地將優(yōu)質(zhì)實(shí)驗(yàn)方案與結(jié)果交到客戶手上。美迪西可以提供抗體全流程服務(wù),包括:藥物發(fā)現(xiàn)、CMC研究服務(wù)、符合GLP規(guī)范的綜合性臨床前研究服務(wù)(藥效學(xué)研究、藥代動(dòng)力學(xué)評(píng)價(jià)和安全性評(píng)價(jià)等);以合規(guī)、高效、高質(zhì)的服務(wù)助力客戶產(chǎn)品順利獲批等。
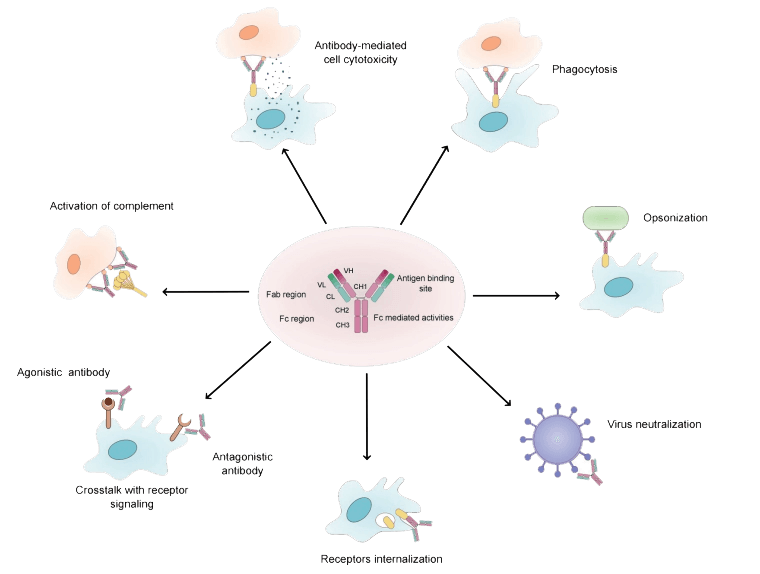
Overview of the natural function of antibodies[1]
 抗體藥物開(kāi)發(fā)
抗體藥物開(kāi)發(fā)- 針對(duì)某個(gè)特定靶點(diǎn)開(kāi)發(fā)創(chuàng)新性抗體藥或抗體相關(guān)藥物的研發(fā)流程中,篩選出合適的候選抗體是其中非常重要的一個(gè)環(huán)節(jié)。目前常見(jiàn)的抗體發(fā)現(xiàn)方法包括雜交瘤技術(shù)、噬菌體展示技術(shù)、單B細(xì)胞抗體篩選技術(shù)等。雜交瘤抗體制備具有10年以上的定制化抗體生產(chǎn)經(jīng)驗(yàn),以及經(jīng)驗(yàn)豐富的抗體藥物研發(fā)團(tuán)隊(duì),美迪西建立了抗體藥物開(kāi)發(fā)平臺(tái)。美迪西雜交瘤研發(fā)服務(wù)可提供多種免疫方法(蛋白、多肽、小分子、全細(xì)胞),確保滿足客戶需求。
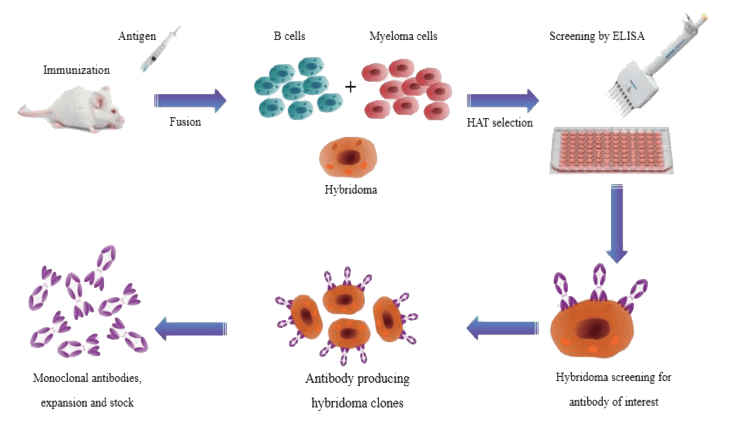
Production route of hybridoma technology[2]
- 納米抗體制備納米抗體諸多方面均優(yōu)于傳統(tǒng)抗體。基于駝科動(dòng)物重鏈抗體的VHH單域抗體的特殊結(jié)構(gòu),兼具傳統(tǒng)抗體與小分子藥物的優(yōu)勢(shì),幾乎完美克服了傳統(tǒng)抗體的開(kāi)發(fā)周期長(zhǎng),穩(wěn)定性較低,保存條件苛刻等缺陷,逐漸成為新一代治療性生物醫(yī)藥與臨床診斷試劑中的新興力量。相比于常規(guī)抗體,納米抗體的優(yōu)勢(shì)有:分子量小,可穿透血腦屏障;原核或真核系統(tǒng)中高表達(dá);特異性強(qiáng),親和力高;對(duì)人的免疫原性弱等。美迪西生物提供駝科動(dòng)物VHH抗體文庫(kù)構(gòu)建服務(wù),包括抗原的制備,免疫,抗體文庫(kù)菌的構(gòu)建以及納米抗體的淘選,ELISA驗(yàn)證等相關(guān)實(shí)驗(yàn)。
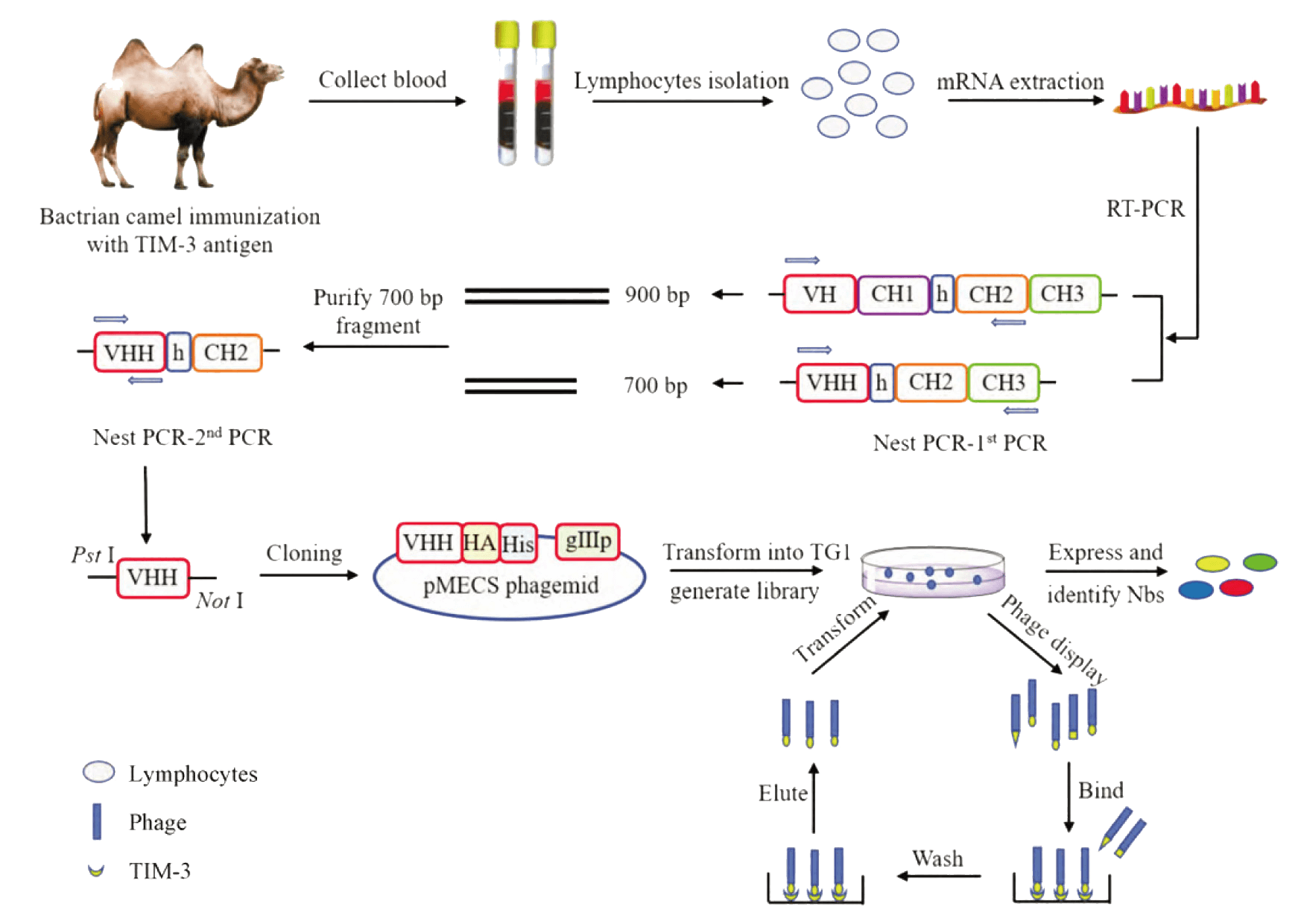
Nanobody production scheme using a phage display library[3]
- 單B細(xì)胞抗體制備美迪西提供單B細(xì)胞抗體制備技術(shù)服務(wù),包括單B細(xì)胞分選和單B細(xì)胞Ig基因轉(zhuǎn)錄,擴(kuò)增,測(cè)序等。單B細(xì)胞抗體制備技術(shù)是目前新型、高效的抗體發(fā)現(xiàn)方法之一,具有速度快、通量高、以及抗體重輕鏈可變區(qū)天然配對(duì)的優(yōu)勢(shì)。

單B細(xì)胞抗體制備流程
- 美迪西案例
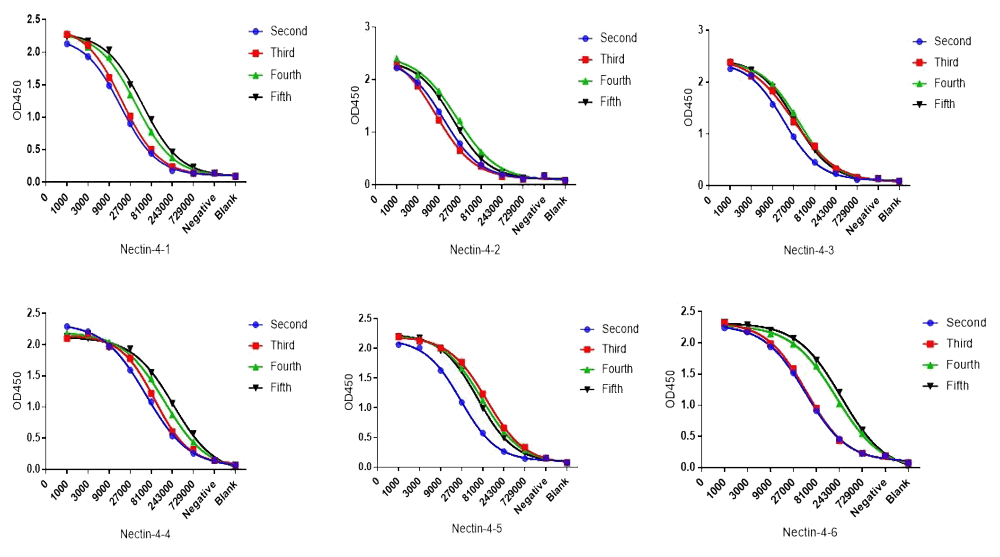
Nectin-4 Mouse Serum Titer

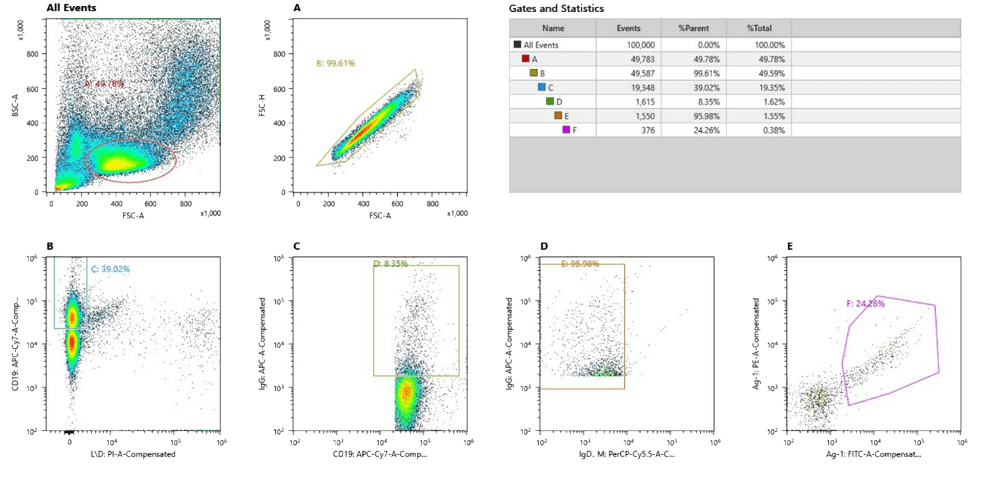
Nectin-4 (4-1) Sorting Single B Cell
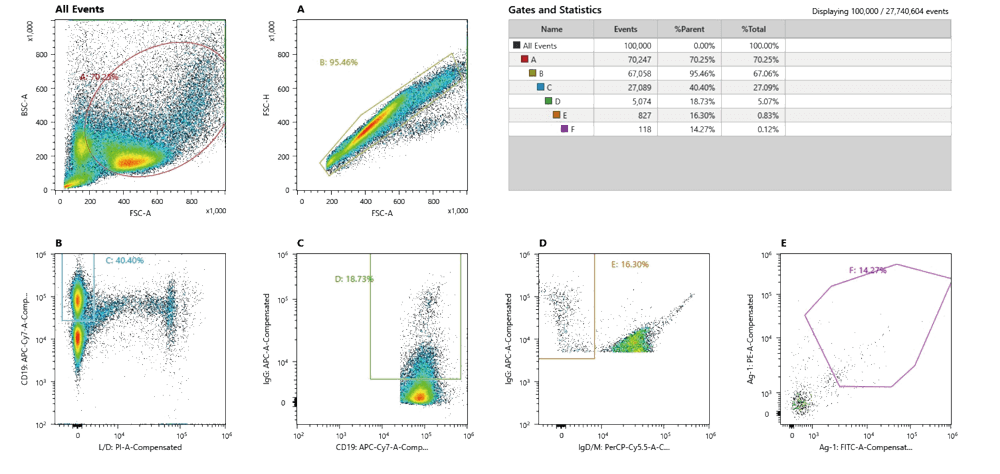
Nectin-4 (4-6) Sorting Single B Cell
- 抗藥物抗體制備高靈敏度及多樣性的多克隆抗藥物抗體可作為免疫原性研究中的陽(yáng)性參照物,模擬ADA在人體中產(chǎn)生的情況,同時(shí)也可以特異性檢測(cè)體內(nèi)抗體藥水平,是藥代動(dòng)力學(xué)研究的重要試劑。因此,抗藥物抗體作為抗體藥物研發(fā)必備工具試劑,其不但是臨床申報(bào)必不可少的試劑之一,在臨床階段也有十分廣泛的應(yīng)用。美迪西在ADA開(kāi)發(fā)方面具有豐富的經(jīng)驗(yàn),已成功交付一百以上訂單,可提供高親和力和特異性的多克隆抗藥物抗體開(kāi)發(fā)服務(wù),服務(wù)周期短,開(kāi)發(fā)成本低。美迪西案例
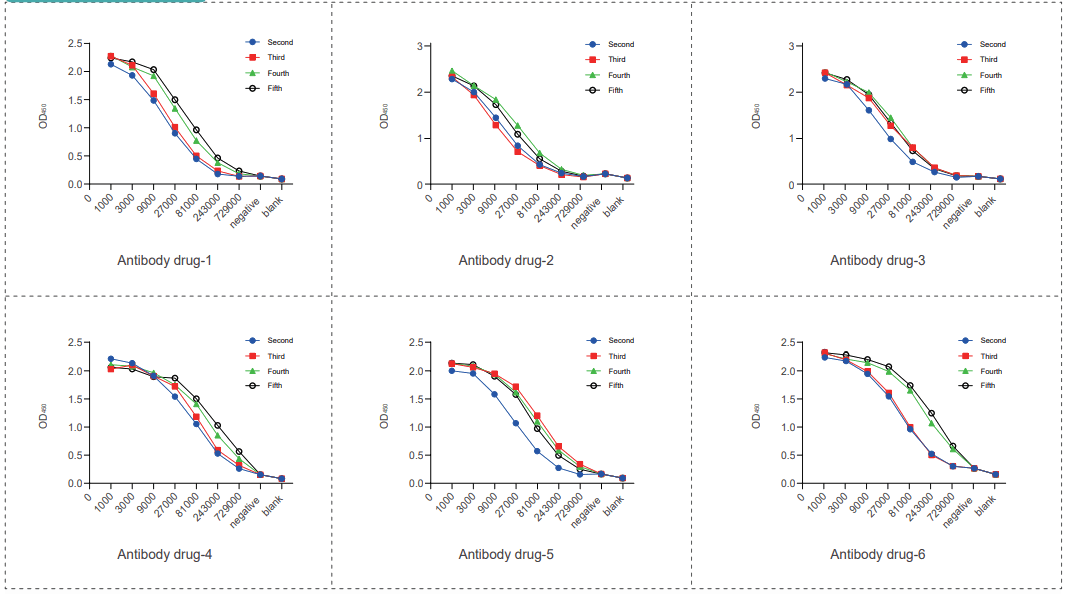
血清效價(jià)

純化后抗體效價(jià)
 抗體藥物體外研究
抗體藥物體外研究- 抗體類藥物的活性測(cè)定是指對(duì)藥物的有效成分、含量及藥物效價(jià)進(jìn)行測(cè)定,在藥物研發(fā)及質(zhì)量控制中至關(guān)重要,是探索藥物作用機(jī)制(MOA),提供藥物IND申報(bào)依據(jù)的重要手段。抗體藥物在與其特定靶點(diǎn)結(jié)合后,通過(guò)激活或阻斷細(xì)胞因子等信號(hào)傳導(dǎo)、補(bǔ)體系統(tǒng)活化及細(xì)胞殺傷等生物學(xué)作用發(fā)揮治療效果。隨著藥物高通量篩選平臺(tái)的不斷建立與生產(chǎn)規(guī)模的不斷放大,基于細(xì)胞系的體外分析方法,例如依據(jù)藥物作用機(jī)制構(gòu)建的報(bào)告基因細(xì)胞株更是因靈敏度高,檢測(cè)周期短,重復(fù)性好且操作簡(jiǎn)單而被廣泛應(yīng)用于新藥開(kāi)發(fā)的過(guò)程中。體外藥理藥效分析需要根據(jù)抗體特點(diǎn),靶點(diǎn)特性來(lái)設(shè)計(jì)相應(yīng)實(shí)驗(yàn),分析方法主要包括基于流式、細(xì)胞成像的細(xì)胞分析;基于ELISA,Luminex等可溶性蛋白的分析。
- 結(jié)合實(shí)驗(yàn) Binding assay (FACS, ELISA, SPR)
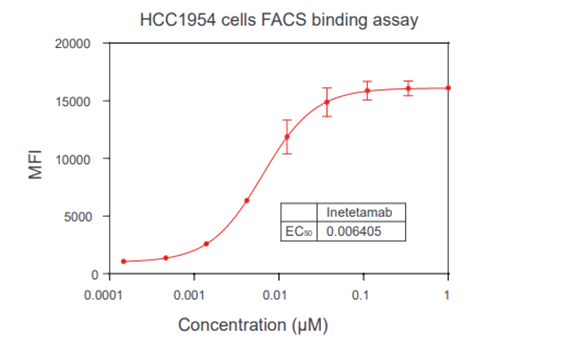 Dose-dependent binding of Inetetamab (anti-HER2) with HCC1954 cells were tested through FACS, the data showed that Inetetamab binds with HCC1954 cells with EC50 of 6.4 nM.
Dose-dependent binding of Inetetamab (anti-HER2) with HCC1954 cells were tested through FACS, the data showed that Inetetamab binds with HCC1954 cells with EC50 of 6.4 nM.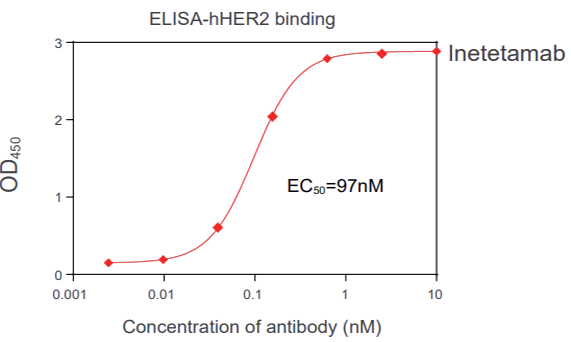 Dose-dependent binding of Inetetamab (anti-HER2) with human HER2 protein were tested through ELISA, the data showed that Inetetamab binds with HER2 protein with EC50 of 97 nM.已驗(yàn)證的靶點(diǎn):PD-1, PD-L1, VEGF, Nectin1, Nectin2, Nectin3, Nectin4, NECL1, NECL2, NECL3, NECL4, NECL5, EPHA1, EPHA2, EPHA3, EPHA4, EPHA5, INSR, IGF-1R, HSA, FcRN, FcRI, FcRII, FcRIII, C1q, Factor B, HER2, Transferrin, EPCR, STAT3, STAT5, STAT1, 4-1BB, SHP2, ATIII, EGFR, gp1, etc.
Dose-dependent binding of Inetetamab (anti-HER2) with human HER2 protein were tested through ELISA, the data showed that Inetetamab binds with HER2 protein with EC50 of 97 nM.已驗(yàn)證的靶點(diǎn):PD-1, PD-L1, VEGF, Nectin1, Nectin2, Nectin3, Nectin4, NECL1, NECL2, NECL3, NECL4, NECL5, EPHA1, EPHA2, EPHA3, EPHA4, EPHA5, INSR, IGF-1R, HSA, FcRN, FcRI, FcRII, FcRIII, C1q, Factor B, HER2, Transferrin, EPCR, STAT3, STAT5, STAT1, 4-1BB, SHP2, ATIII, EGFR, gp1, etc.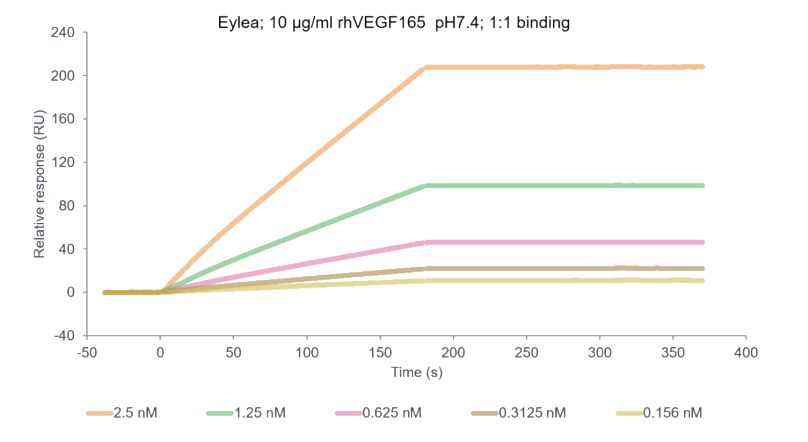 Eylea binding with hVEGF
Eylea binding with hVEGF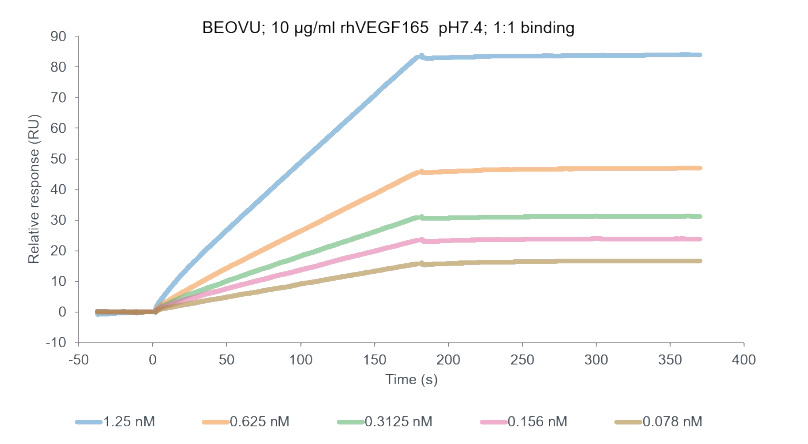 BEOVU binding with hVEGF
BEOVU binding with hVEGF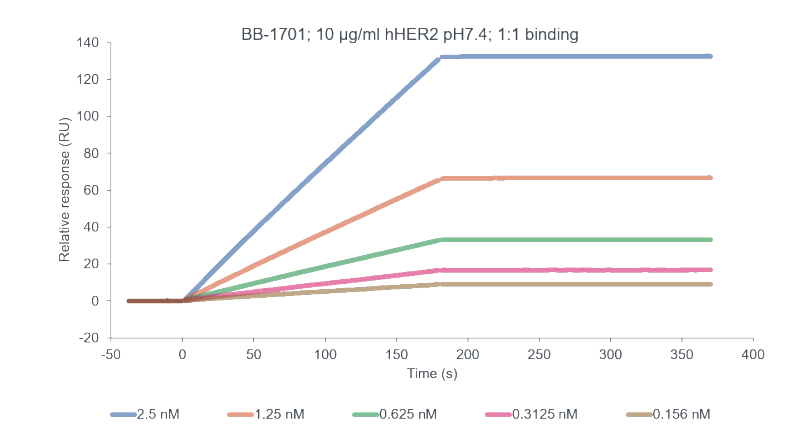 BB-1701 binding with hHER2
BB-1701 binding with hHER2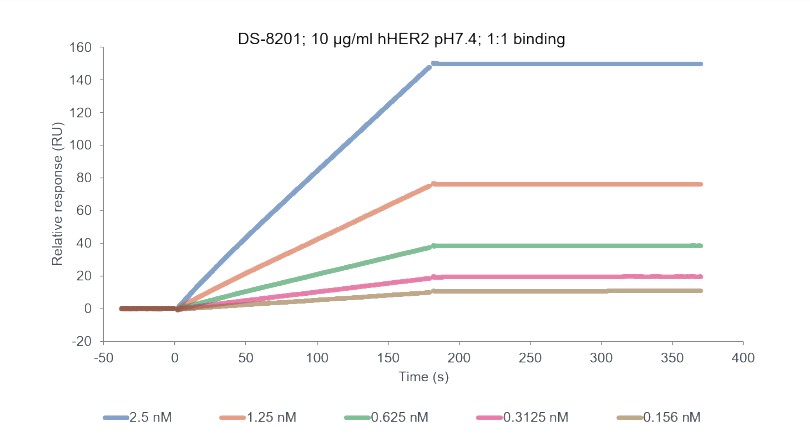 DS8201 binding with hHER2
DS8201 binding with hHER2 - 抗體的功能性實(shí)驗(yàn)
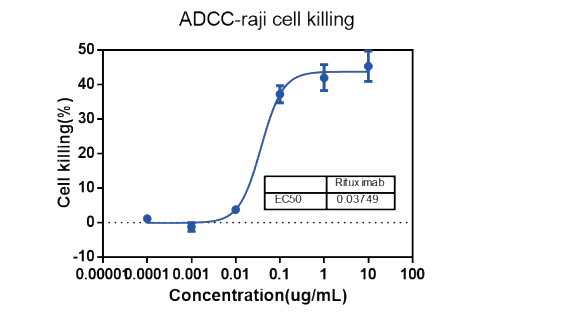 Raji cells were mixed with human PBMCs, and different doses of Rituximab was added to induce ADCC, the killing of raji cells were detected through FACS(CFSE labeling of raji).
Raji cells were mixed with human PBMCs, and different doses of Rituximab was added to induce ADCC, the killing of raji cells were detected through FACS(CFSE labeling of raji).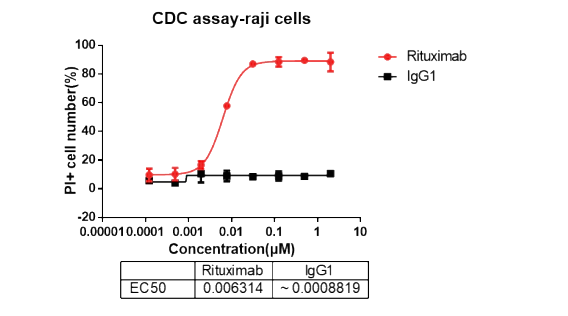 Raji cells were mixed with human AB serum, and different doses of Rituximab was added to induce CDC, the killing of raji cells were detected through FACS(PI staining of raji).
Raji cells were mixed with human AB serum, and different doses of Rituximab was added to induce CDC, the killing of raji cells were detected through FACS(PI staining of raji).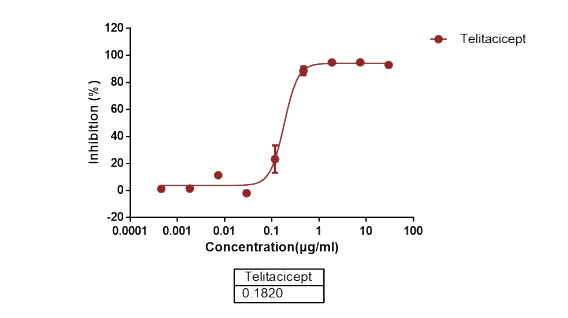 B cells were treated with Teliacicept and induced with Baff for 72 hours, H3-thymidine incorporation were analyzed through scintillation counting.
B cells were treated with Teliacicept and induced with Baff for 72 hours, H3-thymidine incorporation were analyzed through scintillation counting.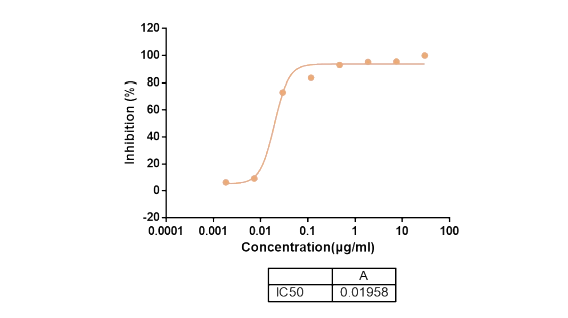 T cells were treated with compound A and induced with ICOSL for 72 hours, H3-thymidine incorporation were analyzed through scintillation counting.
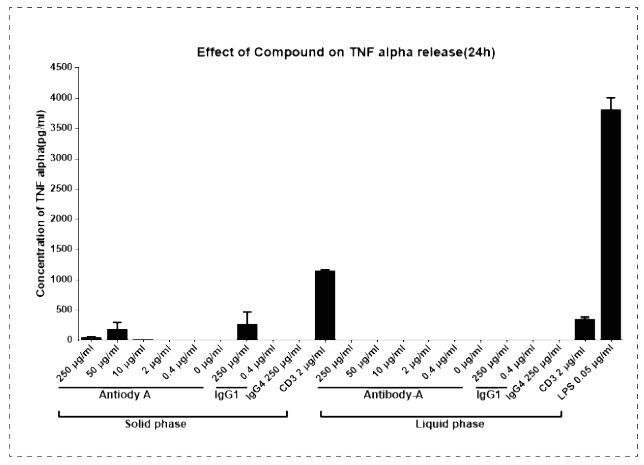
T cells were treated with compound A and induced with ICOSL for 72 hours, H3-thymidine incorporation were analyzed through scintillation counting. - 細(xì)胞因子釋放實(shí)驗(yàn)使用抗體A/IgG1和抗CD3/LPS處理人PBMC細(xì)胞25小時(shí)(液相或固相),通過(guò)Luminex試劑盒分析TNFα水平. 按照ICH指導(dǎo)原則測(cè)定細(xì)胞因子釋放,其中必須測(cè)試的因子有IL-2、IL-6、IL-10、IFN-γ和TNF-α。使用受試抗體處理PBMC細(xì)胞,至少測(cè)試3種。受試抗體的呈現(xiàn)形式包括固相和液相。ELISA、Luminex、CBA 和 MSD 方法可用于檢測(cè)細(xì)胞因子。 OKT3用作陽(yáng)性對(duì)照。 該測(cè)定的目的是評(píng)估潛在的抗體誘導(dǎo)細(xì)胞因子釋放效應(yīng),以防止臨床試驗(yàn)中發(fā)生強(qiáng)細(xì)胞因子釋放風(fēng)暴。
 抗體藥物的CMC研究
抗體藥物的CMC研究- 美迪西可提供抗體藥物工藝開(kāi)發(fā)和制劑研發(fā)服務(wù)。在確保研發(fā)質(zhì)量的基礎(chǔ)上,美迪西團(tuán)隊(duì)通過(guò)嚴(yán)謹(jǐn)?shù)脑囼?yàn)方案設(shè)計(jì)(DOE)、專業(yè)化的研發(fā)技術(shù)、標(biāo)準(zhǔn)化的項(xiàng)目管理、規(guī)范化的試驗(yàn)操作、高效的多方溝通,持續(xù)助力客戶的抗體藥物研發(fā)!
- 美迪西案例:LQ0362022年2月,洛啟生物L(fēng)Q036——重組抗IL-4Rα單域抗體霧化液(畢赤酵母)的IND正式獲得CDE批準(zhǔn)。LQ036是一款針對(duì)中重度哮喘治療的吸入式納米抗體藥物。在LQ036的研發(fā)過(guò)程中,美迪西依托其吸入制劑研發(fā)平臺(tái),參考國(guó)內(nèi)外吸入制劑的指導(dǎo)原則并結(jié)合各國(guó)申報(bào)要求,為L(zhǎng)Q036制定專門(mén)的吸入制劑吸入特性指標(biāo)研究方案,協(xié)助LQ036順利完成了中國(guó)NMPA和澳洲TGA申報(bào)材料的準(zhǔn)備,并成功獲批。
 抗體藥物藥效學(xué)評(píng)價(jià)
抗體藥物藥效學(xué)評(píng)價(jià)- 抗體的動(dòng)物體內(nèi)藥效試驗(yàn)是抗體藥物研究中一項(xiàng)重要的藥理參數(shù),直接反映了抗體的功效并影響臨床試驗(yàn)設(shè)計(jì)。美迪西致力于為客戶提供成熟的評(píng)估抗體體內(nèi)藥效的腫瘤模型,在AAALAC認(rèn)證的環(huán)境下完成模型動(dòng)物的建模和飼養(yǎng),并以GLP-like的高標(biāo)準(zhǔn)完成相關(guān)藥效學(xué)評(píng)價(jià)試驗(yàn)。美迪西多年來(lái)深耕動(dòng)物領(lǐng)域,為藥物研發(fā)提供合適的動(dòng)物模型,可提供多種用于評(píng)估抗體藥物的腫瘤模型及非腫瘤模型,在AAALAC認(rèn)證的環(huán)境下完成模型動(dòng)物的建模和飼養(yǎng),并以GLP-like的高標(biāo)準(zhǔn)完成相關(guān)藥效學(xué)評(píng)價(jià)試驗(yàn)。多種實(shí)驗(yàn)動(dòng)物:嚙齒類:小鼠/大鼠、兔子非嚙齒類:比格犬、小型豬、非人靈長(zhǎng)類動(dòng)物
- 美迪西案例: CD3+ Bispecific Antibody
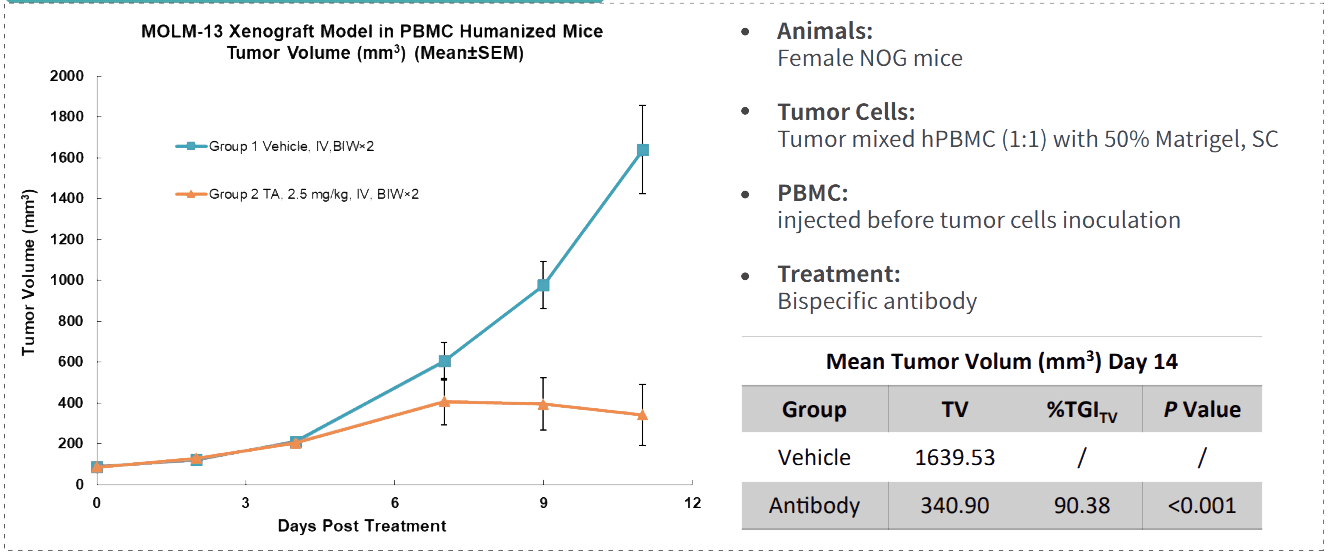
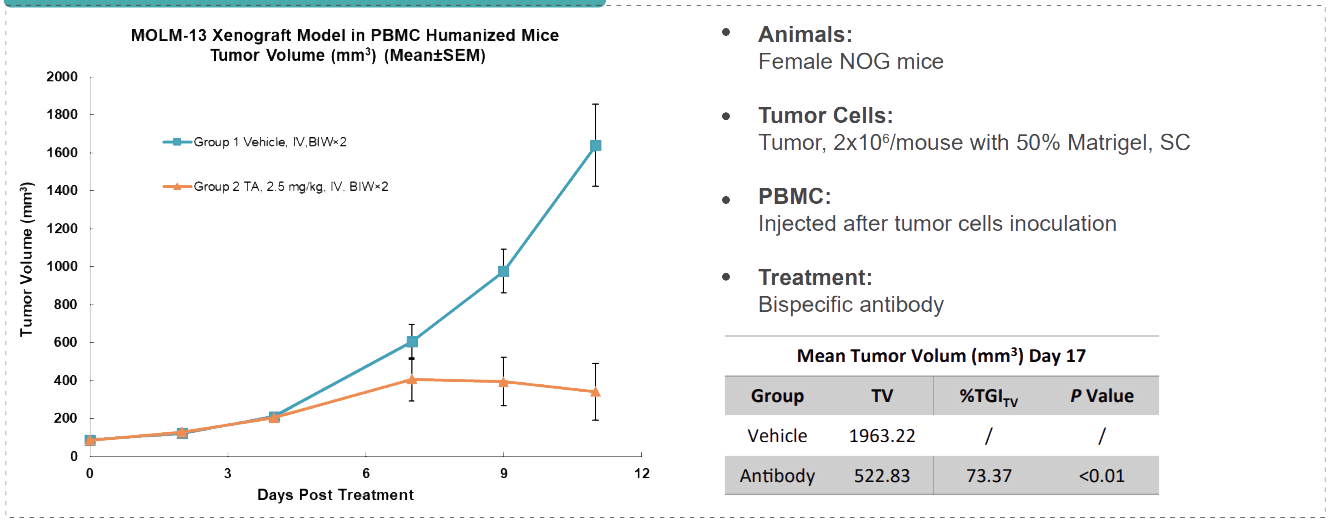
 抗體藥物藥代動(dòng)力學(xué)評(píng)價(jià)
抗體藥物藥代動(dòng)力學(xué)評(píng)價(jià)- 美迪西在抗體藥物體內(nèi)分析中可提供多種測(cè)檢測(cè)方法,通過(guò)分析動(dòng)物體內(nèi)采集的血漿/血清樣本,為客戶提供可靠?jī)?yōu)質(zhì)的PK數(shù)據(jù)。美迪西案例: Pharmacokinetics of YYB-101 in cynomolgus monkeys在四只雄性食蟹猴中單次靜脈注射 YYB-101(劑量為10 mg/kg)后,研究其藥代動(dòng)力學(xué)特征。血清Tmax為2 h,Cmax為221.57 μg/mL,AUC(0–∞)為94 802.96 μg/mL*h。 t1/2Z 約為 21.7 天,清除率為 0.11 mL/kg/h。這項(xiàng)實(shí)驗(yàn)是通過(guò)美迪西進(jìn)行的。
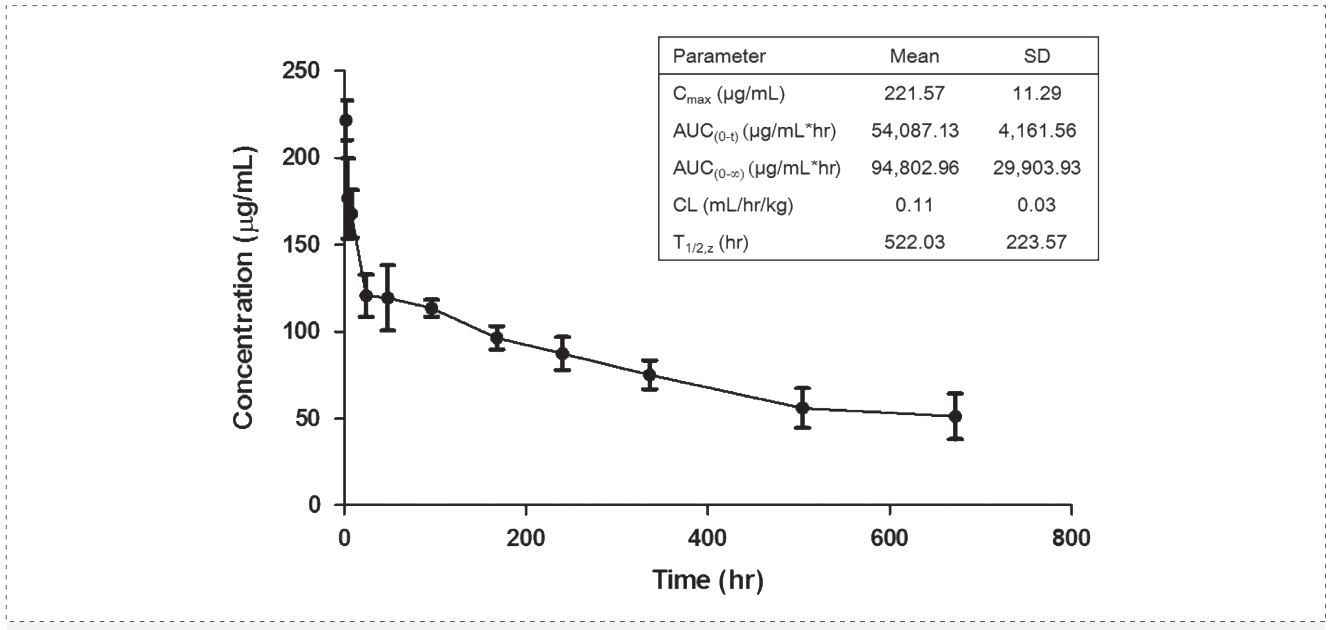
Pharmacokinetic profile of YYB-101 in cynomolgus monkeys[4]
美迪西案例: Anti-drug antibodies of YYB-101 in cynomolgus monkeys在每天服用YYB-101(劑量為 50mg/kg )的第一天,在一只雌性猴子中檢測(cè)到抗藥物抗體,但在第 29 或 85 天從該動(dòng)物收集的樣本中未檢測(cè)到抗藥物抗體。僅在 1 只動(dòng)物中檢測(cè)到抗藥物抗體。單一時(shí)間點(diǎn),幾乎沒(méi)有觀察到與正常組織的交叉反應(yīng)。 這項(xiàng)研究通過(guò)美迪西進(jìn)行。基于這些結(jié)果,一項(xiàng)針對(duì)晚期實(shí)體瘤患者的 I 期臨床研究正在進(jìn)行中 (NCT02499224)。
 抗體藥物安全性評(píng)價(jià)
抗體藥物安全性評(píng)價(jià)- 美迪西毒理研究部遵循ICH指導(dǎo)原則S6和S9,結(jié)合每一個(gè)項(xiàng)目的具體情況定制個(gè)性化的安全性評(píng)價(jià)方案,提供符合NMPA、FDA、OECD、TGA等國(guó)際GLP標(biāo)準(zhǔn)的安全性評(píng)價(jià)服務(wù),包括單次和重復(fù)給藥毒性試驗(yàn)(伴隨毒代動(dòng)力學(xué)研究) 安全藥理(包括組織交叉反應(yīng))免疫原性檢測(cè)
- 美迪西案例: Toxicokinetics of YYB-101 in cynomolgus monkeys靜脈注射YYB-101后,YYB-101的平均全身暴露量(AUC0-168h)和Cmax值隨劑量成比例增加。在每周輸注 YYB-101 四次后,YYB-101 的平均血清峰濃度和谷濃度趨于穩(wěn)態(tài)。最后一次給藥后 63 天,康復(fù)動(dòng)物的血清濃度可量化(第 22 天起約為 Cmax 的 2.8%)。重復(fù)靜脈注射YYB-101后,全身暴露量(AUC0-168h)增加,累積率為2.38至2.95。這項(xiàng)研究通過(guò)美迪西進(jìn)行的。

Toxicokinetic parameters on days 1 and 22 following intravenous infusion of YYB-101 at 10, 50, or 200 mg/kg perday in cynomolgus monkeys[4]
 美迪西部分助力抗體項(xiàng)目案例
美迪西部分助力抗體項(xiàng)目案例- BAT6021注射液和BAT6005注射液2021年9月,百奧泰BAT6021注射液和BAT6005注射液創(chuàng)新藥接連獲批臨床,在腫瘤治療領(lǐng)域取得新進(jìn)展。BAT6021和BAT6005是百奧泰開(kāi)發(fā)的抗TIGIT單克隆抗體,用于腫瘤治療。作為長(zhǎng)期合作伙伴,美迪西先后為百奧泰創(chuàng)新藥BAT6021、BAT6005提供(包括藥代和安全性評(píng)價(jià)在內(nèi)的)綜合性臨床前研究服務(wù),為百奧泰新藥項(xiàng)目的臨床獲批助力。
- BAT7104注射液2021年10月,百奧泰PD-L1/CD47雙抗BAT7104注射液獲臨床試驗(yàn)?zāi)驹S可,本次獲批的適應(yīng)癥為晚期惡性腫瘤。BAT7104是靶向PD-L1/CD47的雙特異性抗體藥物,旨在抑制PD-1/PD-L1和CD47/SIRP-α途徑。美迪西作為百奧泰長(zhǎng)期合作伙伴,有幸在BAT7104注射液的研發(fā)中與百奧泰合作,在GLP的實(shí)驗(yàn)室環(huán)境和操作規(guī)范下,完成了BAT7104注射液的(包括藥代動(dòng)力學(xué)和安全性評(píng)價(jià)在內(nèi)的)綜合性臨床前研究服務(wù),為BAT7104注射液高效、高質(zhì)的獲批臨床提供了專業(yè)保障。
- JYB19042022年5月,濟(jì)民可信旗下子公司江蘇濟(jì)燁生物制藥有限公司lgE抗體藥物JYB1904注射液獲批臨床。JYB1904是一款新型抗IgE重組人源化單克隆抗體靶向治療藥物。JYB1904注射液具有優(yōu)良的臨床治療潛力,可為中重度哮喘等過(guò)敏性疾病的臨床治療提供潛在的新方案。美迪西為該藥提供了符合GLP規(guī)范的(包括藥代和安全性評(píng)價(jià)在內(nèi)的)綜合性臨床前研究服務(wù),在攻堅(jiān)克難中賦能JYB1904項(xiàng)目成功 獲批。
- CC3122022年6月,惠和生物首個(gè)靶向CD19/CD3/CD28三特異性抗體CC312的IND申請(qǐng)獲得FDA默示許可,這是國(guó)內(nèi)首個(gè)、全球第三個(gè)基于CD28 共刺激信號(hào)進(jìn)入臨床研發(fā)階段的三特異性抗體,CC312在針對(duì)血液瘤的臨床前研究中表現(xiàn)出顯著的藥效學(xué)作用及良好的安全性。在本次獲批中,美迪西為CC312提供了符合GLP規(guī)范的(包括藥代和安全性評(píng)價(jià)在內(nèi)的)綜合性臨床前研究服務(wù),以合規(guī)、高效、高質(zhì)的服 務(wù)助力其順利獲批。
- BAT20222022年6月, 百奧泰注射用BAT2022獲得臨床試驗(yàn)批準(zhǔn)。注射用BAT2022是百奧泰自主研發(fā)的雙特異性中和抗體,擬用于治療由于新冠病毒及其突變株感染引起的新冠肺炎。在注射用BAT2022的臨床前研發(fā)中,美迪西依托豐富的項(xiàng)目經(jīng)驗(yàn)和扎實(shí)的專業(yè)基礎(chǔ),在極短時(shí)間內(nèi)向百奧泰呈遞了完整的試驗(yàn)方案。最終在GLP的實(shí)驗(yàn)室環(huán)境和操作規(guī)范下,完成了注射用BAT2022的安全性評(píng)價(jià)研究服務(wù),以合規(guī)、高效、高質(zhì)的服務(wù)助力其成功獲批臨床,為注射用BAT2022的快速獲批臨床提供了專業(yè)保障。
- GT900082022年10月,開(kāi)拓藥業(yè)PD-L1/TGF-β雙靶點(diǎn)抗體(GT90008)獲批臨床。GT90008是一款PD-L1/TGF-β雙靶點(diǎn)抗體,可以同時(shí)抑制PD-L1和TGF-βR2的高度活性,具有成為同類最佳藥物的潛力。在GT90008的研發(fā)中,美迪西依托蛋白質(zhì)/抗體藥代動(dòng)力學(xué)研究平臺(tái)和生物技術(shù)藥物非人靈長(zhǎng)類安全評(píng)價(jià)技術(shù)服務(wù)平臺(tái),提供了符合GLP規(guī)范的(包括藥代和安全性評(píng)價(jià)在內(nèi)的)和藥代的綜合性臨床前研究服務(wù),整個(gè) 項(xiàng)目的研發(fā)進(jìn)展順利且高效。
- HCW92182022年10月,HCW Biologics Inc.融合蛋白復(fù)合物HCW9218獲FDA批準(zhǔn)進(jìn)行癌癥治療試驗(yàn)。HCW9218是一種異源二聚體、雙功能融合蛋白復(fù)合物,包含TGF-β受體II的細(xì)胞外結(jié)構(gòu)域和IL-15/IL-15受體α復(fù)合物,能有效激活和增殖NK細(xì)胞和CD8+ T細(xì)胞,增強(qiáng)細(xì)胞對(duì)腫瘤靶標(biāo)的細(xì)胞毒性,優(yōu)化化療的療效并減少化療副作用。美迪西作為HCW的合作伙伴,在GLP的實(shí)驗(yàn)室環(huán)境和操作規(guī)范下,建立了適用于 HCW9218的分析方法,提供了臨床前藥代和安評(píng)研究,全力促成該項(xiàng)目的高質(zhì)高效完成。此外,美迪西臨床前藥理及毒理研究團(tuán)隊(duì)依托在軟件、技術(shù)、規(guī)范、素質(zhì)等各方面全面成熟的SEND數(shù)據(jù)轉(zhuǎn)換平臺(tái),助力HCW9218成功申報(bào)FDA,推動(dòng)其進(jìn)入臨床試驗(yàn)階段。
- NB0022023年7月,邏晟生物NB002順利通過(guò)FDA審查并同意開(kāi)展Ⅰ期臨床試驗(yàn)。NB002是一款靶向TIM-3獨(dú)特表位的單克隆治療抗體,具有顯著的單藥抗腫瘤的治療效果,其不僅顯著激活T和NK細(xì)胞的活性,增強(qiáng)其對(duì)抗腫瘤的能力,更重要的是NB002重建了腫瘤環(huán)境中被抑制的天然免疫,恢復(fù)DC細(xì)胞反應(yīng)能力,提高髓系細(xì)胞抗原遞呈功能,整體性解除TIM-3調(diào)控的從天然免疫到獲得免疫的抑制性作用,有效地增 強(qiáng)腫瘤免疫殺傷能力。美迪西作為邏晟生物的合作伙伴,為NB002提供了安全性評(píng)價(jià)、藥代動(dòng)力學(xué)等臨床前研究服務(wù),助力其IND申請(qǐng)順利獲FDA臨床許可。
- 參考文獻(xiàn):[1] Ivana Spasevska. An outlook on bispecific antibodies: Methods of production and therapeutic benefits.
[2] Abdullah F U H Saeed, et al. Antibody Engineering for Pursuing a Healthier Future. Front Microbiol. 2017 Mar 28;8:495. doi: 10.3389/fmicb.2017.00495.
[3] MA Lin-lin, et al. Construction and screening of phage display library for TIM-3 nanobody. Acta Pharmaceutica Sinica 2018, 53 (3): 388-395.
[4] Hyori Kim, et al. Preclinical development of a humanized neutralizing antibody targeting HGF. Exp Mol Med. 2017 Mar 24;49(3):e309. doi: 10.1038/emm.2017.21.