上半年化藥報產(chǎn)數(shù)據(jù)揭底1類新藥布局升溫
化學藥注冊分類改革對行業(yè)發(fā)展無疑有深遠影響。自2016年3月發(fā)布《化學藥品注冊分類改革工作方案》對化學藥注冊進行新分類,至今已過一年有余。
行業(yè)立項情況究竟如何變化?為此,筆者對2017年上半年化學藥生產(chǎn)申報相關數(shù)據(jù)進行分析。2017年上半年,生產(chǎn)申服依然以化學藥申報為主,沒有中成藥報產(chǎn),也沒有化學藥新2類報產(chǎn)。
新1類: 2個替尼
化藥新1類(1類新藥)有2個報產(chǎn),都是替尼類,分別為正大天晴藥業(yè)集團股份有限公司和南京愛德程寧欣藥物研發(fā)有限公司申報的鹽酸安羅替尼膠囊,以及和記黃埔醫(yī)藥(上海)有限公司申報的呋喹替尼膠囊。
另外,生物藥1類新藥也有一個報產(chǎn),為康希諾生物股份公司和中國人民解放軍軍事醫(yī)學科學院生物工程研究所共同申報的重組埃博拉病毒病疫苗。
鹽酸安羅替尼膠囊此前已啟動的臨床項目適應癥包括晚期非小細胞肺癌、小細胞肺癌,晚期甲狀腺髓樣癌、分化型甲狀腺癌,以及晚期軟組織肉瘤、結直腸癌、晚期腎細胞癌、軟組織肉瘤、晚期胃癌、晚期胃食管結合部腺癌、食管鱗癌。鹽酸安羅替尼膠囊以與現(xiàn)有治療手段相比具有明顯治療優(yōu)勢和重大專項為由被納入優(yōu)先審評品種名單。重組埃博拉病毒病疫苗同樣以創(chuàng)新藥注冊申請和重大專項被納入優(yōu)先審評品種名單。
呋喹替尼膠囊暫未申報優(yōu)先審評,呋喹替尼膠囊已啟動的臨床項目適應癥包括結直腸腫瘤(CRC)、實體惡性腫瘤、非小細胞肺癌和晚期胃癌。
新3類: 以注射劑為主
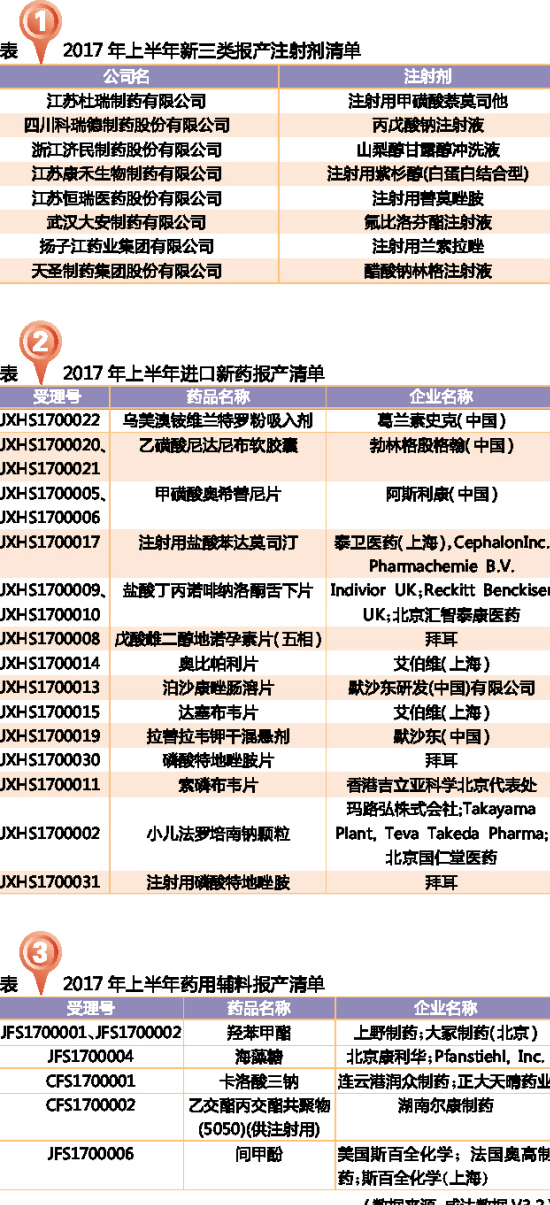
化學藥新3類以原料藥和注射劑申報為主。
注射用紫杉醇(白蛋白結合型)是近幾年比較熱的產(chǎn)品,2016年后申報生產(chǎn)的廠家有石藥集團歐意藥業(yè)有限公司、江蘇康禾生物制藥有限公司和江蘇恒瑞醫(yī)藥股份有限公司。2017年江蘇恒瑞醫(yī)藥股份有限公司以舊6類報產(chǎn)。石藥集團歐意藥業(yè)有限公司和江蘇恒瑞醫(yī)藥股份有限公司都獲得優(yōu)先審評的資質。江蘇康禾生物制藥有限公司2017年以新3類報產(chǎn),預計申報的是未在國內上市的規(guī)格。
恒瑞報產(chǎn)的注射用替莫唑胺適應癥為新診斷的多形性膠質母細胞瘤成人患者,以及用亞硝基脲和甲基芐肼常規(guī)治療后復發(fā)或進展的間變性星形細胞瘤成人患者。恒瑞2015年曾以舊化學藥分類3.3報產(chǎn),止步于第一批床自查核查,本次以新3類再次報產(chǎn)。注射用替莫唑胺已完成臨床的還有江蘇奧賽康藥業(yè)有限公司。替莫唑胺口服藥2016年樣本醫(yī)院市場為4.8億元。
止步于第一批床自查核查再次報產(chǎn)的還有武漢大安制藥有限公司首仿氟比洛芬酯注射液,原是第一家首仿報產(chǎn),現(xiàn)在被重慶藥友制藥有限責任公司2016年“超車”申報而排到第二位。氟比洛芬酯注射液2016年樣本醫(yī)院市場為6.2億元。武漢大安制藥有限公司產(chǎn)品如果能上市,將改變目前北京泰德獨家的格局。
新4類、舊6類: 首仿依然是熱點
新4類和舊6類的報產(chǎn)則以口服藥為主。有搶首仿的,如阿哌沙班片、達沙替尼片、維格列汀片和來那度胺膠囊,正大天晴藥業(yè)集團股份有限公司、四川科倫藥業(yè)股份有限公司和江蘇豪森藥業(yè)股份有限公司在競爭阿哌沙班片,江蘇豪森藥業(yè)股份有限公司和齊魯制藥有限公司在搶仿維格列汀片,達沙替尼片2017年僅石藥集團歐意藥業(yè)有限公司申報,來那度胺膠囊的申報方僅正大天晴藥業(yè)集團股份有限公司。
2016年CFDA批準的首仿藥產(chǎn)品,2017年也有不少廠家加入競爭行列,如富馬酸替諾福韋二吡呋酯片,有安徽貝克生物制藥有限公司和蘇州特瑞藥業(yè)有限公司2家申報。
進口藥(新5.1類): 13個報產(chǎn)
2017年,共13個國內未上市的進口新藥報產(chǎn)(新化學藥分類5.1類)。其中最快獲批的當屬阿斯利康的甲磺酸奧希替尼片,2月承辦3月就獲批了。
進口仿制藥的報產(chǎn)(新化學藥分類5.2類)以原料藥為主,唯一的制劑申報是韓美的吸入用鹽酸氨溴索溶液,這也是第一批臨床自查核查撤回后的“回鍋肉”,目前國內也僅韓美報產(chǎn)。吸入用鹽酸氨溴索溶液目前國內已啟動臨床的有瑞陽制藥有限公司、云南龍海天然植物藥業(yè)有限公司和吉林四環(huán)制藥有限公司。
藥用輔料報產(chǎn)有新的受理號模式,進口的前三位字母為“JFS”,國產(chǎn)的前三位字母為“CFS”。2017年上半年共5個藥用輔料報產(chǎn)。

分享到:









 相關新聞
相關新聞