



業務咨詢
中國:
Email: marketing@medicilon.com.cn
業務咨詢專線:400-780-8018
(僅限服務咨詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(781)535-1428(U.S.)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




2023年3月24號,美迪西生化學部高級副總裁馬興泉博士在IDC2023第四屆化學新藥與改良型新藥研發論壇中做了主題為《小核酸藥物研發中的藥物化學》的報告。

馬興泉 博士 美迪西化學部高級副總裁
中國科學院上海有機化學研究所生命有機國家重點實驗室獲得博士學位,美國國家衛生研究總署(NIH)訪問學者,曾擔任美國斯克利普斯研究所(TSRI) 副研究員。擁有20多年企業藥物研發經驗。馬博士背景是糖化學,在糖化學與生物學領域有較為廣泛的研究,對中草藥活性成分皂甙的分離、提取以及化學合成積累了較為豐富的知識和經驗,對前沿領域的多糖大分子綴合物例如糖脂、糖肽、糖蛋白的合成以及生物活性有多年的研究與積累。在國內外核心期刊發表20多篇學術論文,包括JACS, ANGEW, LANGMUIR, OBC, JMCL等。馬博士2018年加入美迪西,搭建南匯研發中心團隊,領銜創建了美迪西PROTAC、ADC、小核酸等藥物研發平臺, 對多個前沿藥物研發領域有深入的鉆研和見解。
小核酸藥物的發展基于1940年DNA的發現,在這八十多年的時間里有以下幾個關鍵的節點:
1998年FDA批準了首款ASO藥物Fomivirsen,用于治療巨細胞病毒(CMV)視網膜炎;
2004年全球首款核酸適配體藥物Macugen獲批上市,靶向VEGFR,用于治療老年濕性黃斑變性;
2018年全球首款 siRNA藥物Onpattro (Patisiran)由FDA批準上市,用于由 hATTR 引起的多發性神經病患者的治療。
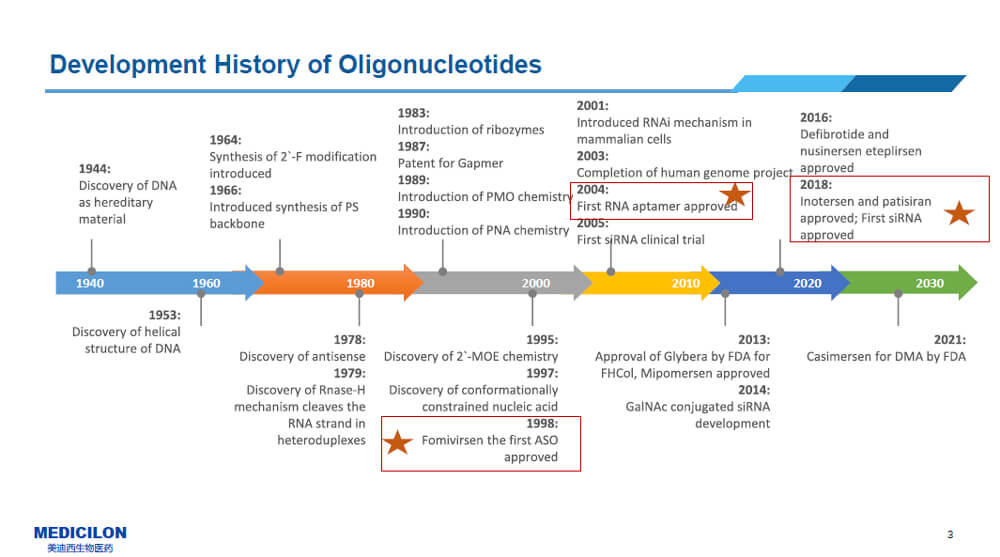
可以看到小核酸藥物的發展歷史稱得上厚積薄發,而且最近小核酸藥物的火熱已經超出了PROTAC和ADC,成為藥物研發屆的新寵兒。因為小核酸藥物的機制是在遺傳物質的根本層面解決問題,這一點對比傳統小分子藥物和抗體藥物具有巨大的優勢,所以隨著對小核酸藥物的開發不斷深入,未來會有更多的曾經認為不可成藥的靶點被攻克。
小核酸藥物包括siRNA, miRNA, Antisense oligo, CpG oligo, Aptamer等,其藥物研發過程并不像我們想象的那么復雜,它其實是一個很簡單直觀的皆是可以通過藥物化學方法合成的化學藥物,所以小核酸藥物的藥物研發主要圍繞化學合成和化學修飾這兩個重心。
截至目前,已經有16款小核酸藥物獲批上市,主要以ASO為主,但近幾年siRNA的數量有增加趨勢,其中肝靶向的小核酸藥物比較多,應用范圍也更廣泛。
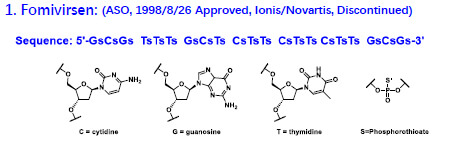
第一個小核酸藥物Fomivirsen,也就是之前說的1998年的第一個ASO藥物,與天然核苷酸相比,對2位的羥基進行了脫氧,用硫取代了磷酸上的氧,這就是小核酸藥物中最基礎的化學修飾,被稱為第一代化學修飾的磷酸骨架修飾。
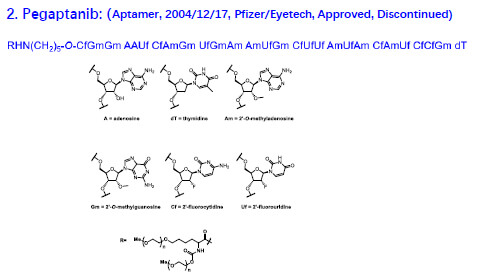
2004年的第一個適配體藥物Pegaptanib在核糖上加了一個甲氧基。

2016年獲批上市的PMO藥物Eteplirsen中用以連接的磷酸修飾成了磷-氮,與之類似的PMO已經有3個獲批上市
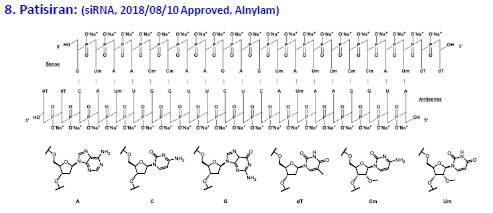
2018年獲批上市的Patisiran是第8個成功上市的核酸藥物,也是第一個siRNA,由于它是雙鏈的RNA結構,所以化學結構上明顯比ASO和PMO要復雜得多。
在這段時間里,除了siRNA橫空出世,用乙二醇對單體進行修飾改造的小核酸藥物上市比較集中,這也是第二代化學修飾。
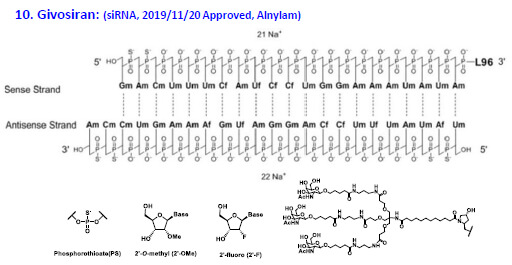
2019年的Givosiran是第一個用到GalNAc遞送系統的siRNA,對于整個核酸藥物的研發具有劃時代的意義。不同于之前LNP脂質體遞送系統,GalNAc的三個氨基半乳糖顯示出了高度的選擇性和靶向性,在肝臟中具有靶點特異性。
目前還有一種在研的是cEt Containing Gapmer,結構比較復雜,仍處在探索研究階段。
對小核酸藥物進行化學修飾有利于提高藥物的穩定性、利用度,甚至對藥效藥代也有提升。隨著對化學修飾技術的更新換代,小核酸藥物的藥物活性也得到了不斷地提升,主要體現在給藥頻率和劑量上。
現在遞送系統的種類也越來越多,這里統計展示了9種遞送系統:
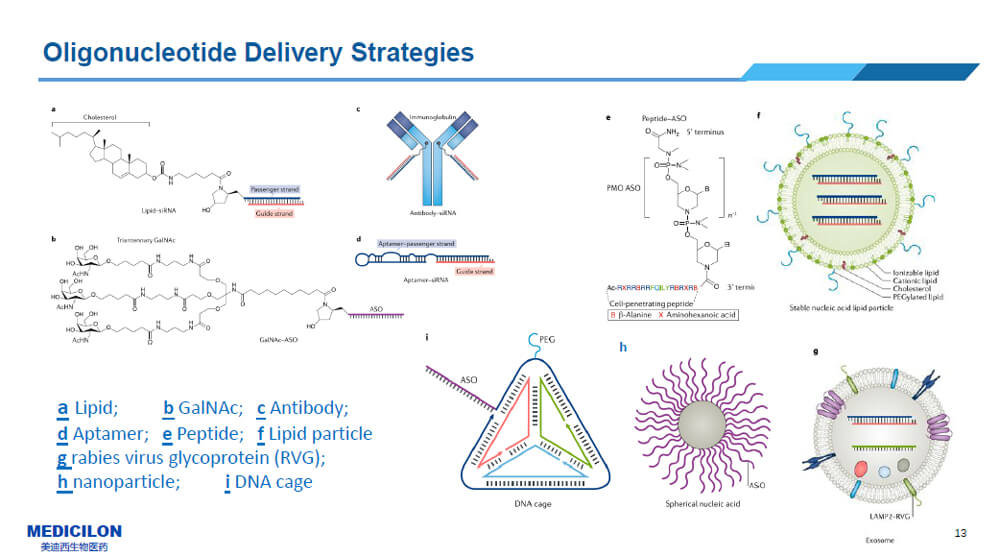
這里很多種類型還沒有經過市場的成功檢驗,像第三種用抗體橋接做siRNA的遞送系統目前還沒有上市的藥物,但已經有很多人在研究了。我們重點還是講講LNP和GalNAc。
LNP在人體內具有免疫原性且為改變性狀的脂質體不能靶向遞送藥物,LNP中膽固醇占比較大,因為微觀結構上看,膽固醇的骨架大,水溶性比較弱,能撐起球形、盤型的結構。
GalNAc不表現出免疫原性,所以更加安全。GalNAc靶向肝細胞上的ASGPR位點,可通過內吞作用被吸收,副作用更小。
美迪西核酸藥物研發服務平臺是集成了藥物發現、生產和臨床前研究的一體化綜合性平臺,可以完成核酸藥物的化學合成和修飾、體內外pkpd的檢測。經過將近4年的研發歷程,美迪西核酸藥物研發服務平臺積累了豐富的經驗,目前有超過10個的on going項目,超過50個致力于核酸藥物研發的化學家組成科研團隊,構建了超過100個可使用的單體。
基于嚴謹的科學態度、開放的技術平臺、豐富的研發經驗和先進的儀器設備,我們可以滿足行業對于前沿創新核酸藥物的研發需求
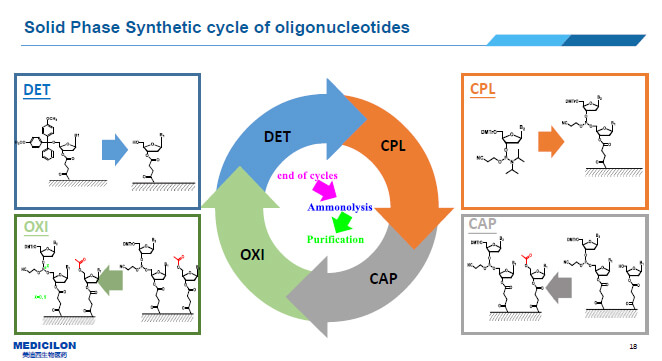
總體來說,每新增一個堿基需要經歷一下4個步驟:DET、CPL、CAP、OXI。
1. 脫保護(Deprotection, DET):將預先連接在固相載體CPG上的活性基團被保護的核苷酸與三氯乙酸反應,脫去其5'-羥基的保護基團DMT,獲得游離的5'-羥基;
2. 縮合連接(Coupling, CPL):將亞磷酰胺保護核苷酸單體與活化劑四氮唑混合,得到核苷亞磷酸活化中間體,與溶液中游離的5'-羥基發生縮合反應;
3. 加帽反應(Capping,CAP):縮合反應中可能有極少數5'-羥基沒有參加反應(少于2%),可用乙酸酐和1-甲基咪唑終止合成,這種短片段可以在純化時分離掉;
4. 氧化穩定(Oxidation, OXI):在氧化劑的作用下,亞磷酰形式轉變為更穩定的磷酸三酯,使DNA磷酸骨架更穩定。
重復以上循環直到需要合成的堿基全部連接完成,然后進入Ammonolysis氨解反應。
氨解反應通過不同的儀器也有兩種反應,一種是氣相的,一種是液相的。氨解后需要進行凍干或者超離心,用去離子水洗滌,再進行分析和純化。注意,在這些步驟里,水的含量需要重點關注。因為水的含量如果過高,容易發生副反應,對于結果會產生不良影響。
對于寡核苷酸的分析美迪西主要使用UPLC和HPLC這兩種儀器。HPLC的檢測結果純度一般可以達到80%以上,UPLC和QTOF聯用檢測的純度也是80%以上。這里我們可以看到試驗結果的峰值圖譜,一般小于500 ppm的結果都是準確的。
純化會用到制備HPLC,純化后核酸藥物樣品的濃度能達到98%以上。第二種方法是是用AEX HPLC,陰離子交換高效液相色譜純化的寡核苷酸必須沒有多余的鹽,這一點很容易通過使用脫鹽柱實現。
這是一個合成siRNA的例子:
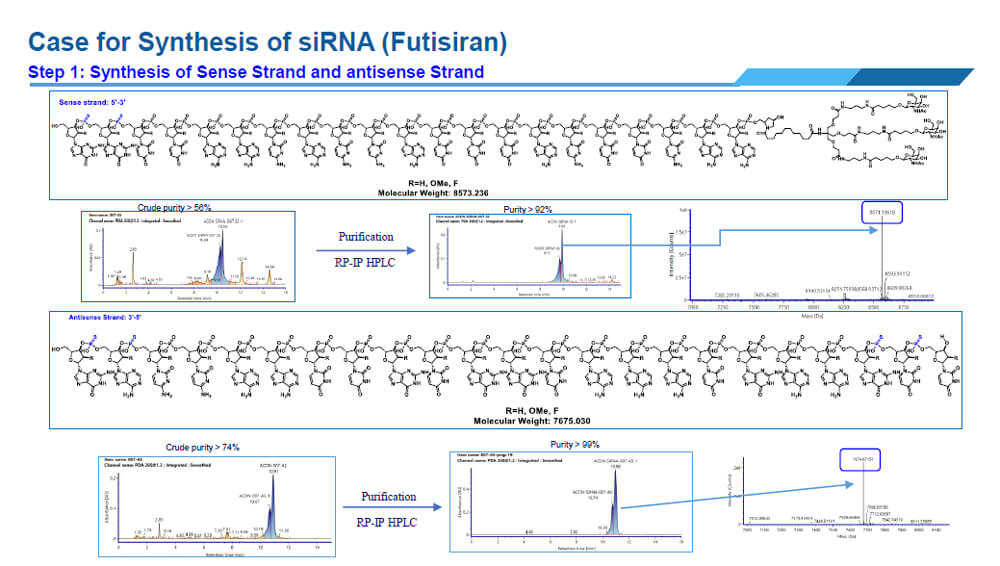
可以看到經過制備HPLC純化后siRNA的純度達到了92%,圖譜上的峰型沒有那么鋒利,事實上這跟最左邊5’上的磷-硫鍵有關,可能出現的手性結構導致數據的結果不完美。
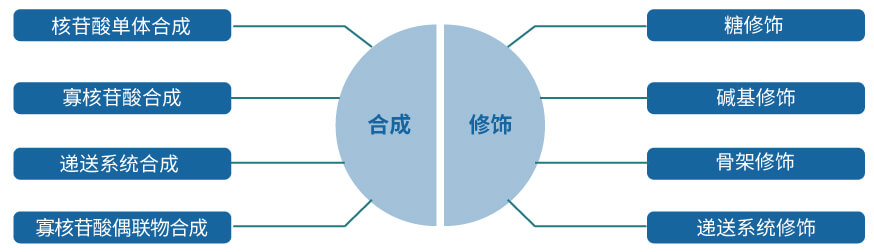
美迪西可以提供單體合成、修飾;寡核苷酸合成;遞送系統合成以及寡核苷酸偶聯物的合成。已經建成的siRNA庫,不僅有豐富的單體庫存,而且擁有龐大的單體合成砌塊庫,可以快速完成各類修飾單體的合成。美迪西擁有專業的小核酸藥物的研發團隊可以提供高效快捷地研發服務;已有多個siRNA藥物FTE項目完成和進行中。
在生物活性評價服務上可以進行:
1. siRNA-GALNAc與靶向肝細胞的結合評估(ELISA,SPR,FP,FACS,MSD,Confocal 顯微鏡)
2. 靶標mRNA/蛋白質水平降低評估(RT/Q-PCR,Western blot)
3. 細胞表型和功能性干擾的評估(細胞增殖,遷移,蛋白質修飾和互作)
4. 脫靶效應評估
核酸藥物作為繼小分子化藥和抗體藥物后的第三大類型藥物,在全球已經形成燎原之勢,發展勢頭迅猛,成為生物醫藥企業研發的重點和熱點。
核酸藥物研發速度極快,靶向性高,有望突破傳統藥物無法解決的“不可成藥”的靶點。在研發過程中,藥物化學是核心和重點。
美迪西核酸藥物研發服務平臺擁有豐富的核酸藥物研發經驗,可以快速完成各類修飾單體的合成,制定開發路線,滿足行業對于前沿創新核酸藥物的研發需求,為醫藥公司及科研單位提供核酸藥物發現、篩選及臨床前研究服務。