



業務咨詢
中國:
Email: marketing@medicilon.com.cn
業務咨詢專線:400-780-8018
(僅限服務咨詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(781)535-1428(U.S.)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




前言
近年來腫瘤免疫治療取得顯著進展,尤其是基于mRNA技術的治療性疫苗,在臨床試驗中展現出卓越療效,為腫瘤防治開辟新途徑。mRNA疫苗通過特異性抗原呈遞有效抑制腫瘤細胞增殖和轉移,結合AI輔助預測系統,有望實現真正的個體化疫苗設計,延長患者無進展生存期。以免疫微環境調控為核心的精準治療新范式,推動腫瘤治療從“廣譜治療”向“個體化醫療”轉變。
美迪西基于成熟的技術平臺和經驗,持續深耕mRNA腫瘤疫苗研發平臺,致力于為客戶提供更快速、更合規、更優質的服務。
制劑分析方法
? RT-qPCR
生物分析方法
? RT-qPCR: mRNA
? ELISA: mRNA表達蛋白;mRNA疫苗免疫原性(效價)
? ELISPOT: IFN-γ水平
制劑安全性研究
? 給藥部位刺激試驗(結合重復給藥毒性試驗進行或單獨開展兔刺激性試驗)
? 豚鼠主動過敏試驗
? 兔體外溶血試驗
組織分布試驗(大鼠)
制劑分析方法
? RiboGreen
生物分析方法
? qPCR: mRNA
? ELISA: mRNA表達蛋白
? ELISPOT: IFN-γ水平
? ECL: ADA
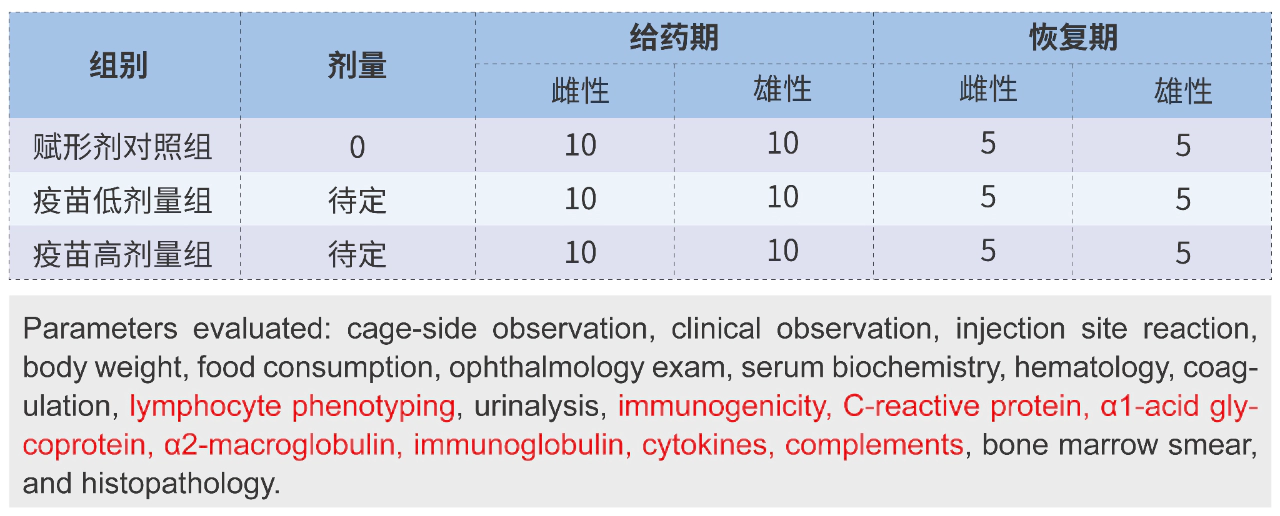
大鼠重復給藥GLP毒性試驗
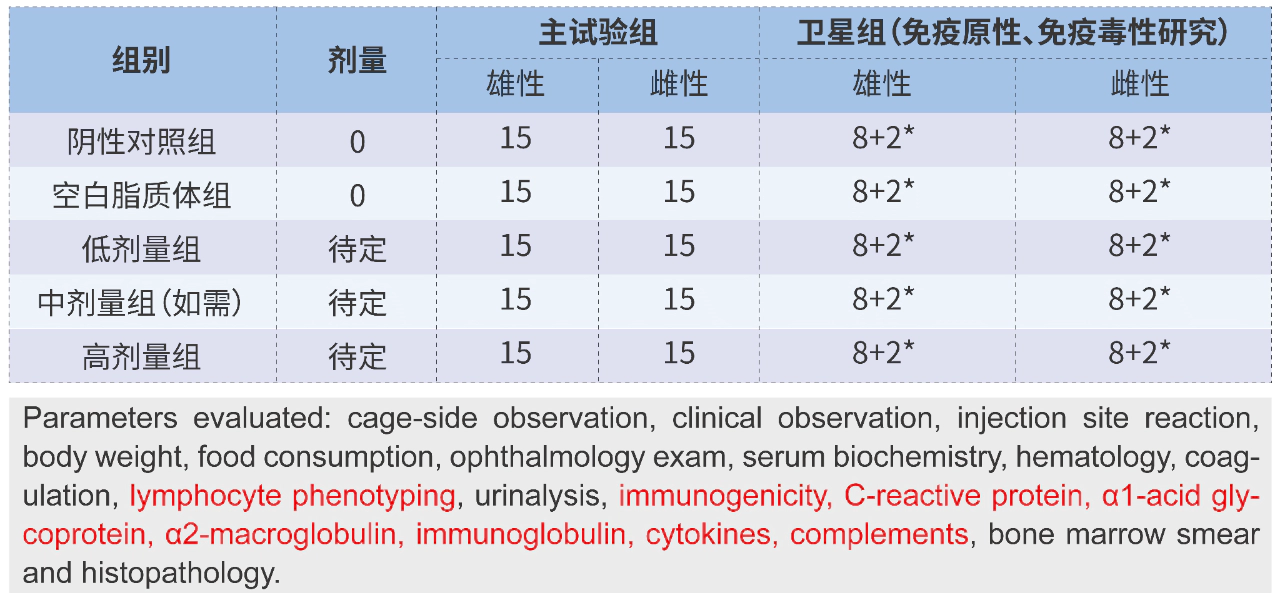
食蟹猴重復給藥GLP毒性試驗
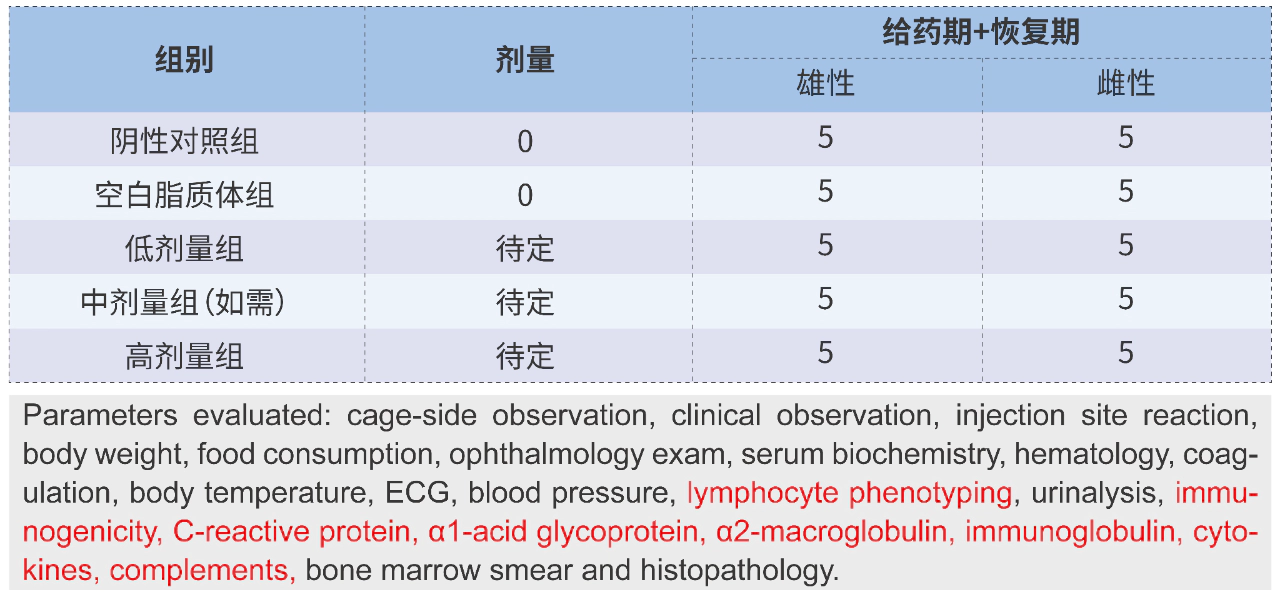
制劑安全性研究
? 給藥部位刺激試驗(結合重復給藥毒性試驗進行或單獨開展兔刺激性試驗)
? 豚鼠主動過敏試驗
? 兔體外溶血試驗
組織分布試驗(大鼠)
安全藥理試驗
? SD大鼠FOB, SD大鼠呼吸系統安全藥理,猴心血管系統安全藥理(伴隨)
一般來說根據制備技術,腫瘤疫苗可分為四類:細胞疫苗、肽類疫苗、病毒疫苗、和核酸疫苗。核酸疫苗是指含有由DNA或RNA編碼的抗原的疫苗。核酸疫苗是一個前景廣闊且極具吸引力的疫苗平臺,因為其可在一次免疫中注射多種抗原,并能夠誘導強烈的MHC-I介導的CD8+ T細胞應答。與傳統疫苗相比,核酸疫苗已顯示出諸多優勢,例如安全性、誘導針對目標抗原的免疫應答的特異性、可同時誘導體液和細胞免疫應答、生產成本相對較低以及易于制造。
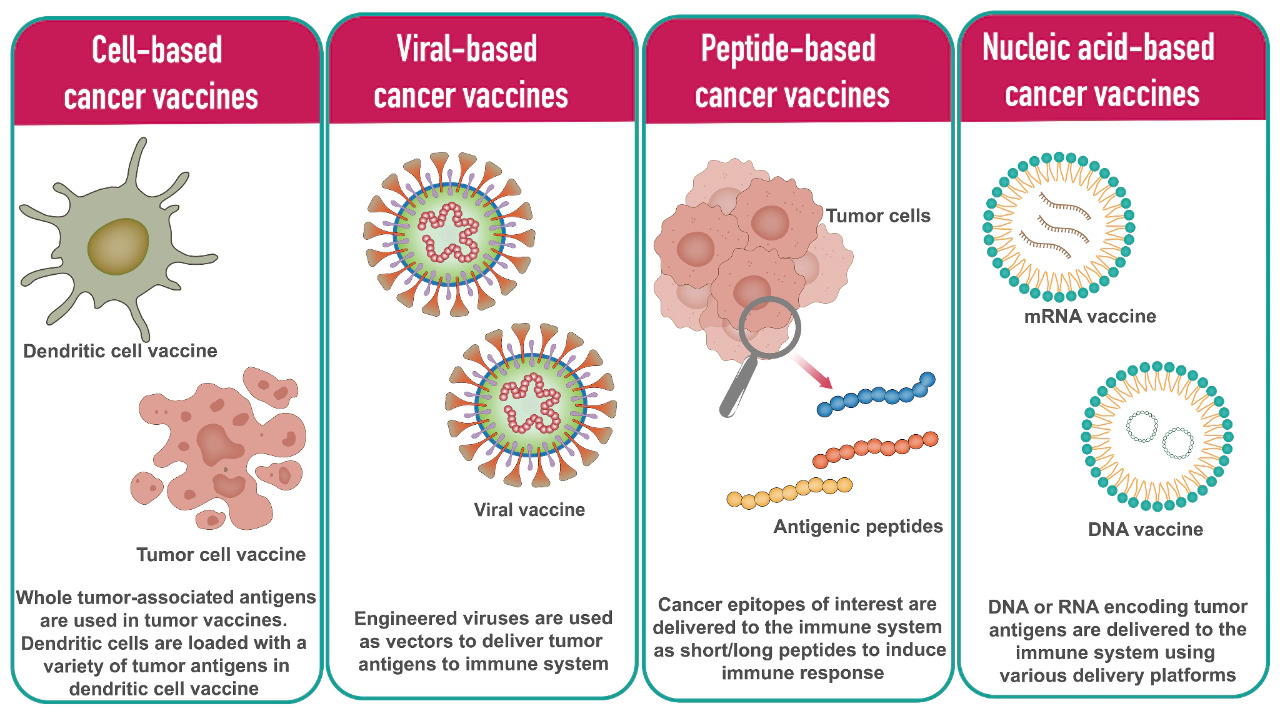
Different types of cancer vaccine platforms[1]
mRNA腫瘤疫苗是一種基于mRNA的免疫療法,能夠編碼腫瘤相關抗原(TAA)或腫瘤特異性抗原(TSA),通過誘導或增強有效的抗腫瘤免疫反應而起效。mRNA疫苗被抗原呈遞細胞內吞并被轉運到細胞質,由核糖體翻譯產生目標抗原蛋白,經過多種途徑刺激機體免疫反應:
(1) MHC-I呈遞途徑
? 細胞內抗原蛋白被蛋白酶體分解成抗原肽表位,通過I類主要組織相容性復合體 (MHC Class I) 運送到細胞表面呈遞給CD8+ T細胞;活化的CD8+ T細胞具備細胞毒性,可特異性殺傷靶細胞
(2) MHC-II呈遞途徑
? 分泌的抗原蛋白可被細胞內吞并降解,通過MHC-II類蛋白運送至細胞表面呈遞給CD4+ T細胞;CD4+ T細胞通過促炎細胞因子激活吞噬細胞,增強其殺傷和吞噬靶細胞的能力,另一方面CD4+ T細胞可以共激活抗原特異性B細胞并誘導體液免疫反應
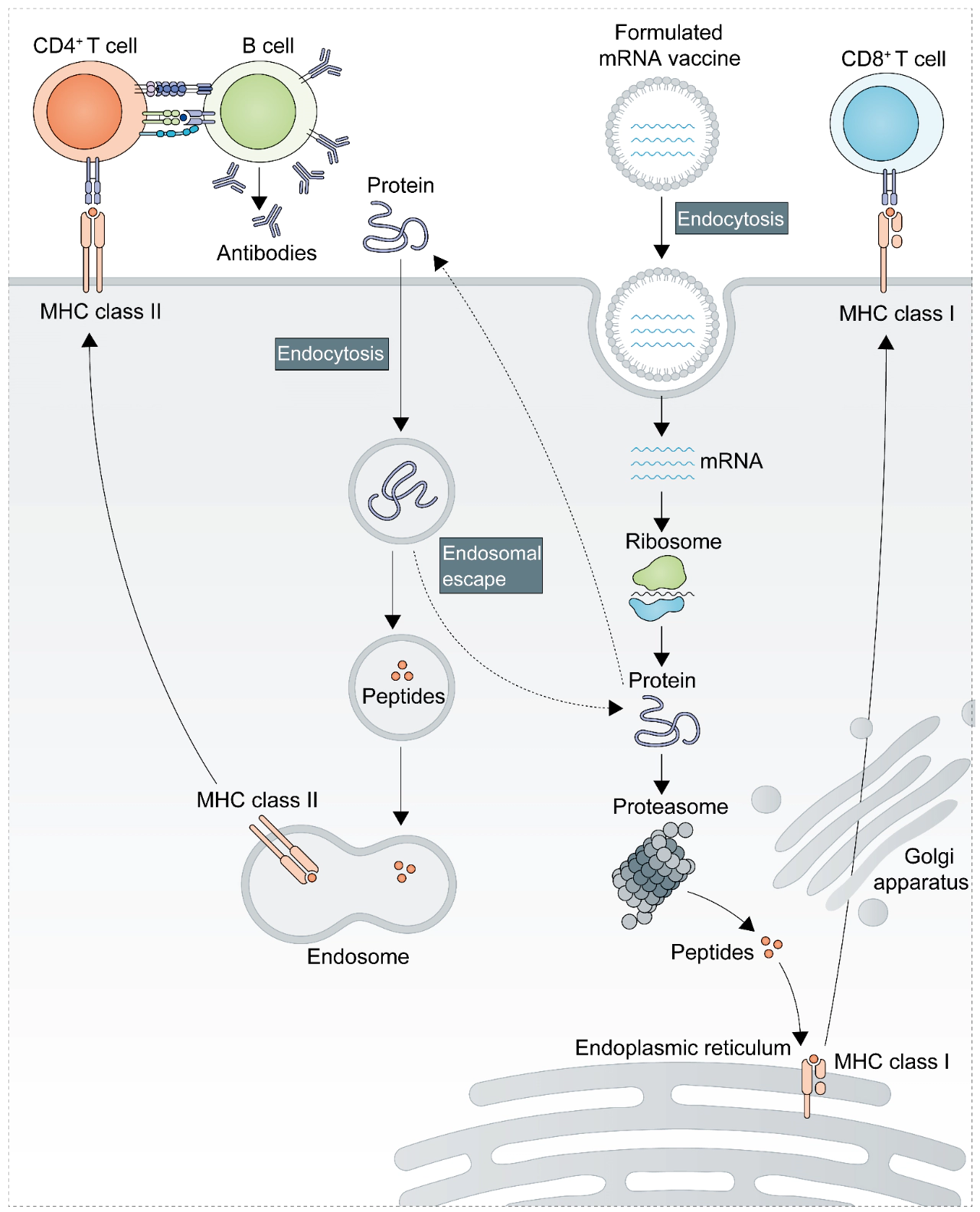
mRNA-based vaccine mode of action[2]
mRNA腫瘤疫苗具有多種優勢,如:
? 抗原選擇范圍廣
? 自佐劑:表現更強的免疫原性
? 安全性:不整合到基因組,安全性高于DNA疫苗
? 生物化學合成,生產過程無病毒感染風險
? 不依賴于細胞培養,構建速度快,借助于人工智能、計算生物學、疫苗學等
已有臨床前和臨床研究證明mRNA疫苗具有抗癌的可行性。目前正在開發各種mRNA腫瘤疫苗用于各種癌癥治療。此外,個性化mRNA疫苗為精準癌癥治療開辟了新的方向。隨著個性化腫瘤疫苗研究和臨床試驗的不斷增加,開發針對不同類型腫瘤的mRNA疫苗的可能性日益增加。
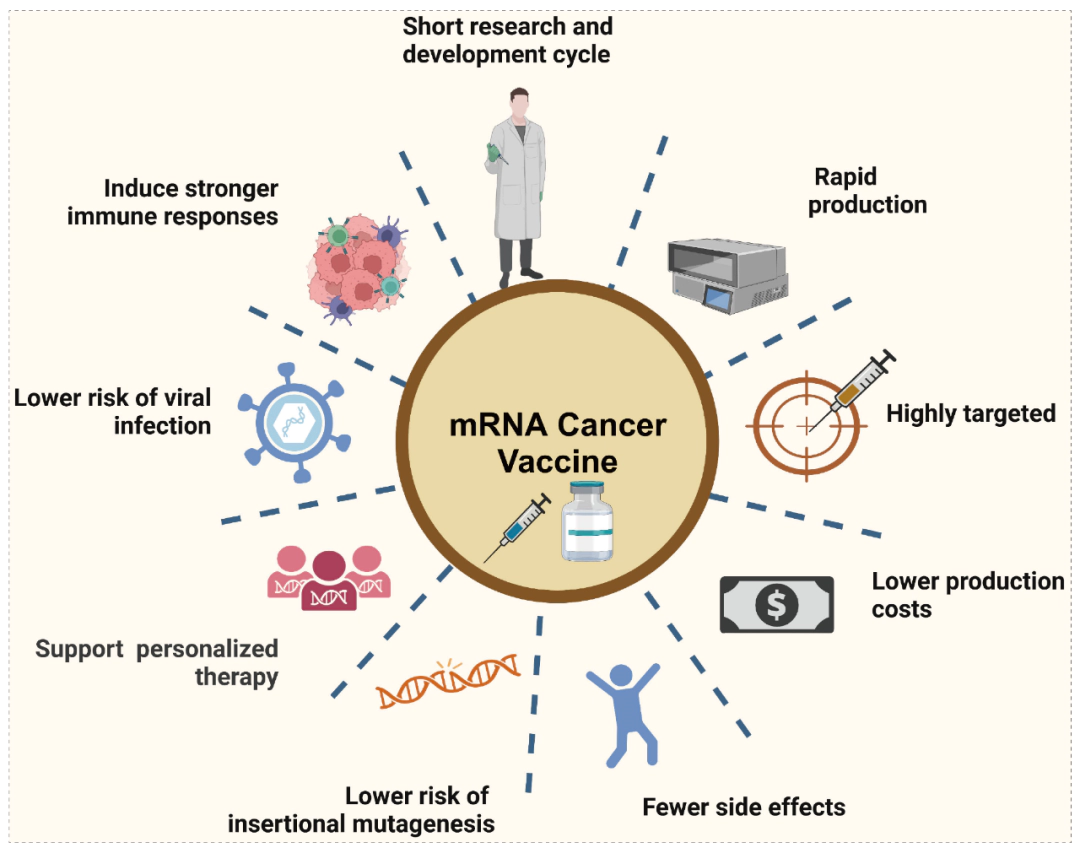
The advantages of mRNA vaccines in the context of cancer therapy[3]
藥學研究階段
? 腫瘤新抗原的識別和篩選
? mRNA核酸序列設計和修飾
? 遞送系統優化
臨床前研究階段
? 動物模型選擇是核心和關鍵
典型的mRNA由一個兩側為5′非翻譯區 (UTR) 的帽子、3′ 非翻譯區 (UTR)、一個編碼mRNA腫瘤疫苗中癌癥抗原的開放閱讀框 (ORF) 和一個poly(A) 尾組成。mRNA的這些成分可以通過修飾來提高穩定性、翻譯效率和免疫刺激特性。設計和優化方法包括編碼區的設計和優化、非編碼區的設計和優化以及遞送形式的設計和優化。
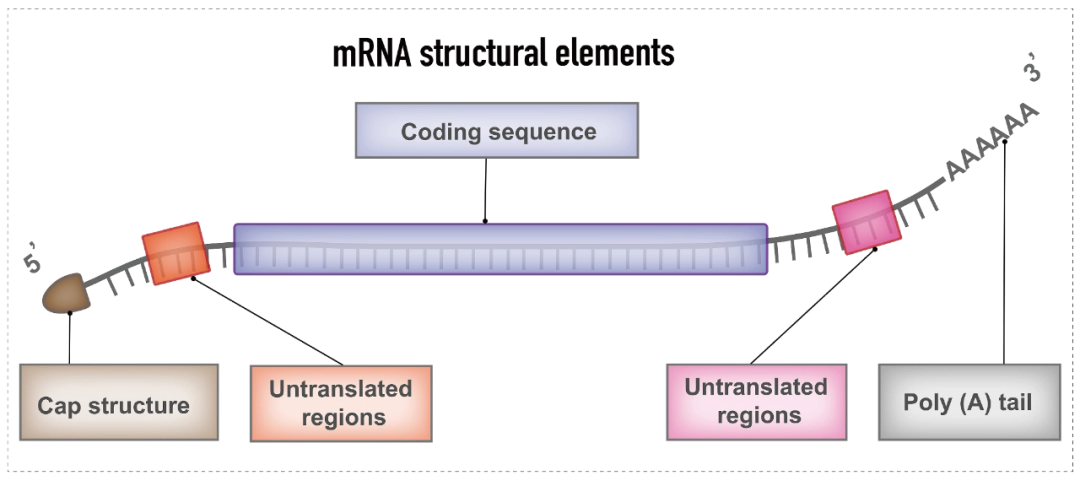
mRNA structural elements[1]
編碼腫瘤抗原的mRNA序列:
優化mRNA的翻譯和穩定性
? 5‘端加帽(5’Cap)和修飾:常見的如通過噬菌體聚合酶將帽類似物(m7GpppG)添加到mRNA的5‘端,提高mRNA的穩定性和翻譯效率;
? 5‘-UTR和3’-UTR修飾:5‘-UTR和3’-UTR包含各種影響mRNA穩定性、翻譯和定位的調控序列;
? 開放閱讀框架(ORF)中的密碼子優化,提高mRNA的穩定性、調控翻譯速度和蛋白質產量;
? Poly(A) tail修飾:Poly(A) tail是基因表達的主要調節因子,通過與5‘ cap協同作用來調節mRNA的翻譯,并參與調節mRNA的穩定性。
免疫原性的調節
? 體外轉錄mRNA的純化、轉錄條件改變、核苷酸修飾、添加額外佐劑等。
疫苗佐劑(可選添加):
? TLR激動劑:如TLR4激動劑MPLA、TLR7激動劑Imiquimod;
? STING激動劑;
? TriMix(一種編碼CD40配體、CD70和TLR4三種蛋白的雞尾酒mRNA);
? 粒細胞巨噬細胞集落刺激因子(GM-CSF);
? 一些mRNA載體,如陽離子脂質和魚精蛋白。
mRNA疫苗的遞送系統:
脂質納米顆粒(LNP)遞送系統
? 目前應用最廣泛的mRNA遞送遞送,主要由可電離的氨基脂質、聚乙二醇、磷脂和膽固醇組成;
? 帶負電荷的mRNA分子可以通過與帶正電荷的脂質的靜電相互作用穩定地輸送到包裹在內核中,而不受細胞外RNase和內體的酶降解。
聚合物載體納米遞送系統
? 多聚體或基于聚合物的核酸載體與LNPs相似,因為多聚體也可以帶正電荷,并通過與mRNA的靜電相互作用來轉染mRNA;
? 常用的聚合物遞送系統如聚乙烯亞胺(PEI)、聚l-賴氨酸(PLL)、聚酰胺胺(PAMAM)、聚β-氨基酯(PBAE)、氨基聚酯。
基于多肽的遞送系統
? 某些帶正電荷的氨基酸能夠通過靜電相互作用吸附mRNA,以及細胞穿透肽(CPPs)能夠快速內化穿過生物膜;
? 魚精蛋白是一種典型的多肽載體,除了穩定地結合mRNA進行遞送外,還可以作為佐劑來激活TLR7/8以誘導先天性免疫反應。
混合納米顆粒遞送系統
? mRNA癌癥疫苗的遞送還可使用多種組分混合制成的載體,例如脂質、聚合物、肽、外泌體和細胞膜等;
? 脂質/聚合物雜化納米粒(LPHNs):一般由可電離脂質、疏水聚合物和聚乙二醇脂質組成,可以通過組分和比例優化實現高轉染效率;
? 陽離子納米乳(CNEs):由脂質和聚合物組成的水包油遞送載體。
病毒載體遞送系統
? 如腺病毒、甲病毒、仙臺病毒、黃病毒和小核糖核酸病毒被用于mRNA的遞送。
DC細胞遞送系統
? DC是早期疫苗研究的重要遞送工具,可以通過電穿孔將主要編碼抗原的mRNA有效地導入DC細胞。
裸mRNA
? 直接注射裸mRNA:由于快速降解和細胞攝取較差,遞送裸mRNA效率低下。
原液質控:mRNA鑒定包括外觀、鑒別、pH值、序列長度、序列完整性及準確性、含量、加帽率、加尾結構或長度和純度等指標。
成品質控:成品階段除常規的疫苗外觀、裝量、pH值、安全性和效力項目外,質控項目主要針對mRNA鑒定(鑒別、含量、純度、完整性),遞送系統各組分鑒定(鑒別、含量),制劑特性項目[包封率、納米顆粒粒徑、分散系數(PDI)、Zeta 電位] 以及工藝相關雜質殘留(有機溶劑等)3個部分。
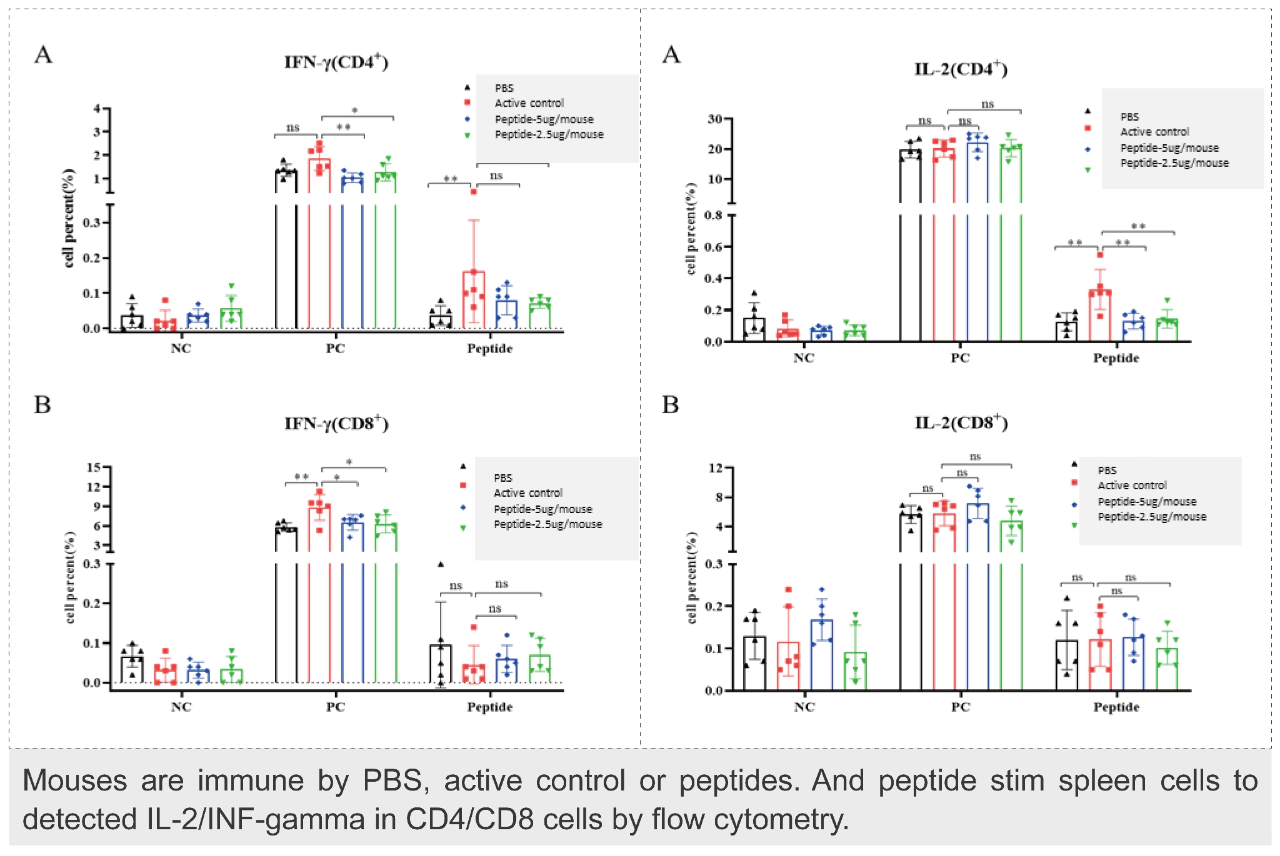
概念驗證測試:mRNA疫苗的臨床前開發需驗證其活性和機制。體外實驗通過共培養T細胞(來自PBMC或全血)與表達TAA的腫瘤細胞系進行。對于靶向TSA的個性化疫苗,因TSA的患者特異性,通常采用多種體外方法,如新抗原的PBMC培養評估,替代商業上難以獲取的合成TSA腫瘤細胞系。
動物模型選擇:動物模型對評估mRNA疫苗的安全性和活性至關重要。通過評估疫苗接種后的抗腫瘤效果、存活率和免疫反應,深入了解作用機制。評估聯合應用mRNA疫苗和檢查點抑制劑的效果,支持未來可能的聯合治療。
模型選擇策略:
? 通用型腫瘤疫苗,確認靶點同源性后,使用鼠源模型
? 個性化腫瘤疫苗,使用鼠源腫瘤細胞構建個性化疫苗,用鼠源模型驗證
? 有MHC限制性的腫瘤疫苗,使用HLA人源化免疫健全小鼠
? 使用靶點人源化小鼠腫瘤細胞完成概念驗證
? 使用HSC免疫系統人源化動物模型進行藥效驗證
體內概念驗證研究:體內概念驗證研究旨在確定活性劑量范圍和最佳給藥方案。通過在小鼠腫瘤模型中評估抗腫瘤作用、存活率、免疫反應或細胞因子誘導,全面了解mRNA疫苗效果,建立免疫原性模型,為臨床試驗提供關鍵信息。
給藥途徑:給藥途徑影響mRNA疫苗的生物分布、持續性、活性持續時間和劑量反應。抗原提呈細胞對mRNA疫苗的攝取、表達和呈遞程度因注射途徑而異,進而影響疫苗的效力和免疫刺激區域。
mRNA疫苗的主要給藥策略包括:
? 皮下注射
? 皮內注射
? 結節內注射
? 肌肉注射
? 靜脈注射
? 腫瘤內注射
? 鞘內注射
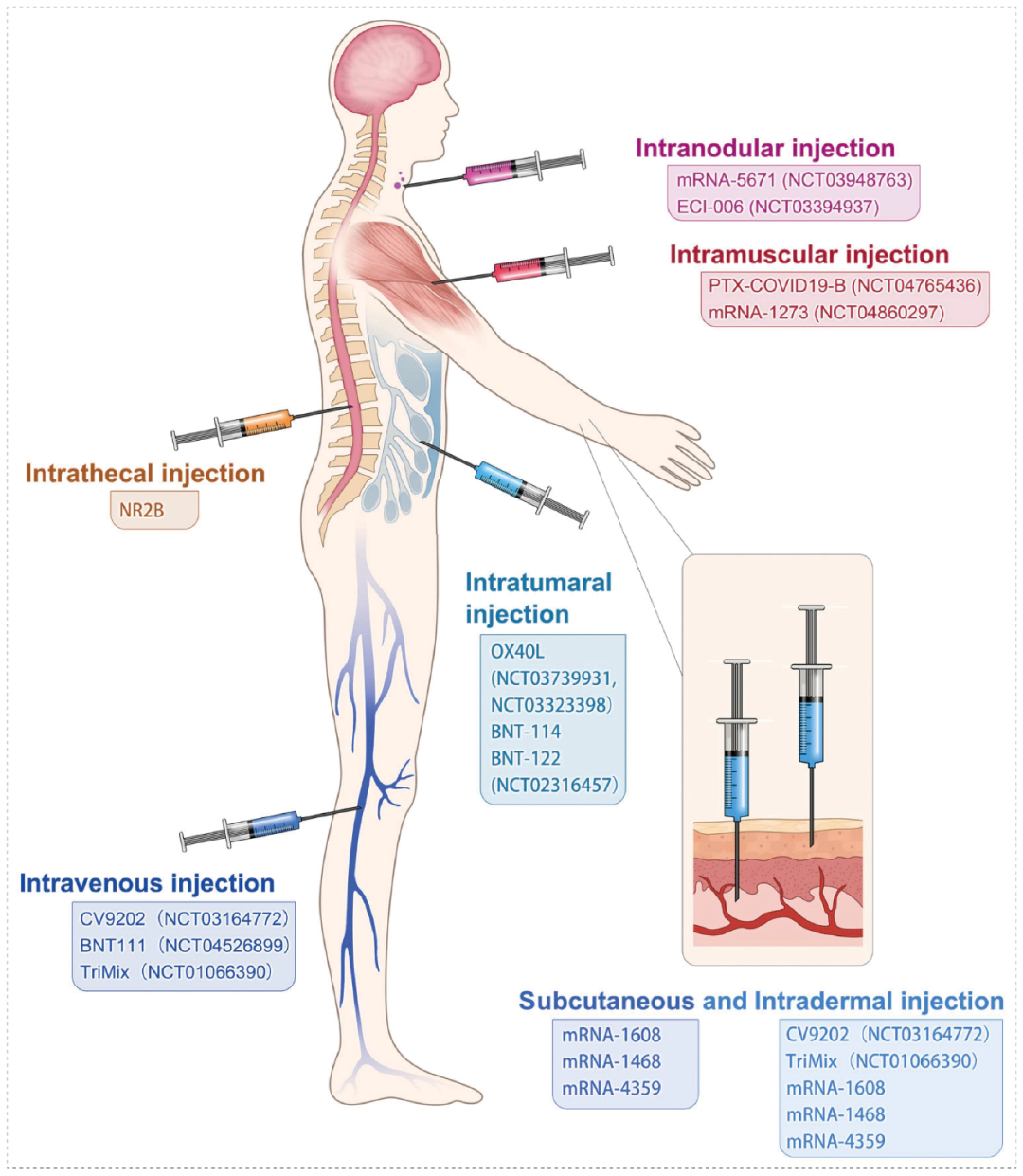
Different strategies for the administration of mRNA vaccines[4]
安全性評價:安全性評價是RNA腫瘤疫苗臨床前開發的關鍵環節,采用嚴格的試驗設計,并且符合GLP標準,確保試驗的科學性以及合規性。使用適當的動物模型模擬人體生理和免疫反應,評估mRNA疫苗的潛在毒性,重點關注動物的臨床表現、體溫變化、相關的炎癥反應、,尤其關注疫苗的遞送系統對肝臟,脾臟等免疫系統或組織的影響,以及對免疫相關指標如淋巴細胞表型、細胞因子、急性反應期蛋白水平(α1和α2)等的影響,為后續臨床試驗提供充分參考。
mRNA腫瘤疫苗在癌癥治療領域顯示出巨大的潛力和希望。隨著技術的不斷進步和臨床驗證的深入,mRNA疫苗已成為一種引人注目的治療選擇。盡管mRNA疫苗在實驗室和早期臨床階段顯示出希望,但它們仍面臨一些挑戰,包括穩定性、遞送系統和免疫原性的問題。未來的研究需要解決這些局限性,例如通過優化mRNA序列、改進遞送載體和增強疫苗的穩定性來提高疫苗的效果和安全性。
mRNA技術的靈活性和可擴展性使其在未來的癌癥治療中具有廣闊的應用前景。結合其他治療方法,如免疫檢查點抑制劑,mRNA疫苗可能提供更有效的治療方案。此外,隨著技術的進一步發展和深入了解mRNA疫苗的生物學機制,未來可能會有更多創新疫苗問世,為癌癥患者提供更多治療選擇。
美迪西具有領先的mRNA腫瘤疫苗研發服務平臺,可為mRNA腫瘤疫苗的開發提供高效優質的解決方案,為各類新型生物技術藥及疫苗的安全性和有效性評價提供全方位支持!
 相關新聞
相關新聞