2015年FDA藥品審評(píng)回顧:新藥批準(zhǔn)創(chuàng)19年來(lái)新高
自上周批準(zhǔn)三款新藥之后,F(xiàn)DA今年的新藥批準(zhǔn)數(shù)量已達(dá)到43個(gè),創(chuàng)下19年來(lái)新藥批準(zhǔn)的新高。目前為止,F(xiàn)DA在2015年批準(zhǔn)的新藥總數(shù)略遜于1996年的45個(gè),當(dāng)時(shí)的這一記錄是在處方藥申請(qǐng)者付費(fèi)法案剛剛實(shí)施4年時(shí)創(chuàng)下的。
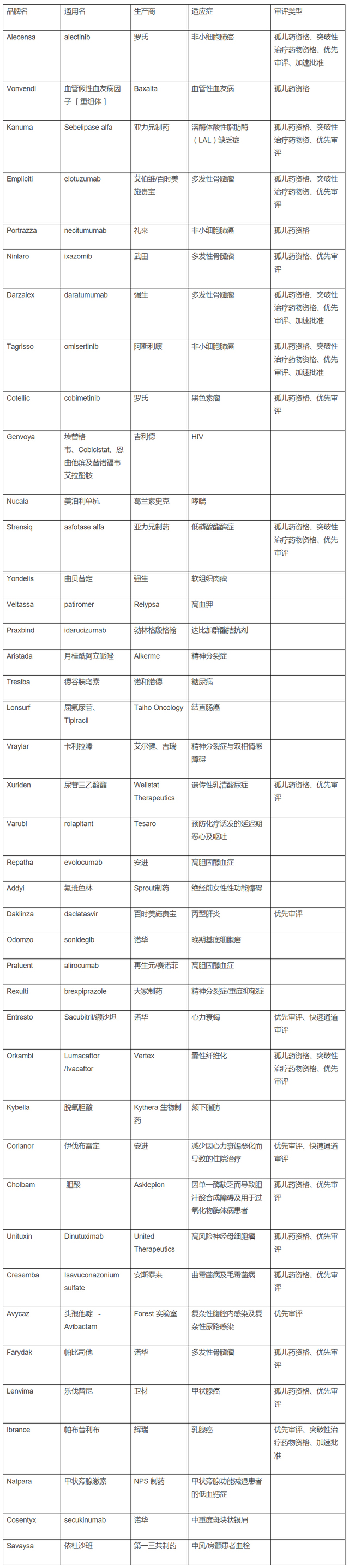
過(guò)去12個(gè)月新藥批準(zhǔn)的名單透露出廣泛的信息,既包含了FDA藥品監(jiān)管審評(píng)的趨勢(shì),也體現(xiàn)了醫(yī)藥行業(yè)的健康發(fā)展,但最能說(shuō)明問(wèn)題的可能是FDA最近批準(zhǔn)的兩款藥物,即亞力兄制藥的Kanuma和Baxalta的Vonvendi,這兩款藥物均為孤兒藥,旨在用于罕見(jiàn)病治療。
由FDA授予孤兒藥資格的治療藥物占到了2015年新藥批準(zhǔn)的逾三分之一,這其中包括一些用于患者人群規(guī)模相對(duì)較小的癌癥治療藥物。此外,最近Kanuma的獲批凸顯了2015年的另一個(gè)重要趨勢(shì),優(yōu)先審評(píng)券在日益升值,優(yōu)先審評(píng)券是因成功開(kāi)發(fā)罕見(jiàn)病藥物而授予藥物生產(chǎn)商的一張快速審評(píng)通行證。亞力兄制藥現(xiàn)在正手握兩張優(yōu)先審評(píng)券,如果該公司選擇將其出售給其它公司,這可能證明有高額的利潤(rùn)。
FDA在批準(zhǔn)新的癌癥治療藥物上保持了其進(jìn)取精神,審評(píng)的速度與以往相比更快。迄今為止,F(xiàn)DA在2015年批準(zhǔn)的癌癥新藥剛好不到批準(zhǔn)新藥總數(shù)的三分之一,批準(zhǔn)的這13款癌癥新藥中,只有3個(gè)藥物未被授予突破性治療藥物資格或一些其它的用來(lái)加快審評(píng)程序的資格。
FDA近來(lái)批準(zhǔn)的多款癌癥治療藥物,如阿斯利康的Tagrisso和強(qiáng)生的Darzalex,這些藥物的批準(zhǔn)均比它們指定的審評(píng)截止日期提前數(shù)月,而在批準(zhǔn)輝瑞帕布昔利布(Ibrance)時(shí)更是采用了加速批準(zhǔn),與審評(píng)截止日期相比提前了一年,僅基于該藥物2期試驗(yàn)數(shù)據(jù)就批準(zhǔn)了這款藥物。
這些藥物的快速批準(zhǔn)不僅得益于FDA的快速審評(píng),同時(shí)也來(lái)自于制藥公司自身的研發(fā)努力,阿斯利康最近批準(zhǔn)的Tagrisso從第一項(xiàng)臨床研究到上市僅僅用了兩年零八個(gè)月。除了新藥,F(xiàn)DA還顯示出對(duì)先前已批準(zhǔn)癌癥治療藥物的適應(yīng)癥擴(kuò)展授予快速審批的意愿,百時(shí)美施貴寶的PD-1抑制劑Opdivo就是一個(gè)最好的例子。
2015年的新藥批準(zhǔn)也看到了競(jìng)爭(zhēng)風(fēng)險(xiǎn),這種風(fēng)險(xiǎn)在一些市場(chǎng)尤其在加大。例如,F(xiàn)DA在過(guò)去一年批準(zhǔn)了四款骨髓瘤新藥,包括上個(gè)月批準(zhǔn)的3個(gè)。今年最備受期待的兩次批準(zhǔn)是PCSK9抑制劑Praluent(再生元制藥/賽諾菲)和Repatha(安進(jìn))。
這兩款藥物在一個(gè)月內(nèi)相繼進(jìn)入美國(guó)市場(chǎng),并在他汀藥物不能充分治療的患者中,對(duì)高膽固醇的降低有相似的有效性與安全性,而這對(duì)于支付者來(lái)說(shuō)是一種利好,他們可通過(guò)對(duì)兩種藥物的施壓而獲得更便宜的藥品定價(jià)。
Praluent和Repatha均被預(yù)測(cè)在未來(lái)某個(gè)時(shí)間點(diǎn)會(huì)成為重磅炸彈級(jí)藥物,2015年批準(zhǔn)的新藥中,有相當(dāng)數(shù)據(jù)的產(chǎn)品可能會(huì)產(chǎn)生逾10億美元的銷售峰值。
強(qiáng)生的Darzalex在臨床研究中繼續(xù)令人印象深刻,與此同時(shí),隨著競(jìng)爭(zhēng)對(duì)手ClovisOncology最近披露數(shù)據(jù),阿斯利康Tagrisso的樂(lè)觀預(yù)期得到提升。在容受了兩年的推遲之后,諾和諾德長(zhǎng)期等待的基礎(chǔ)胰島素-德谷胰島素(Tresiba)終于獲得批準(zhǔn),同時(shí)輝瑞的帕布昔利布第一年上市就報(bào)告了一個(gè)強(qiáng)大的銷售成績(jī)。
從企業(yè)的角度來(lái)看,諾華在今年是多產(chǎn)的一年,該公司有四款新藥獲FDA批準(zhǔn),超過(guò)了其它任何公司。諾華獲批的四款新藥中,Entresto和Cosentyx有望為這家瑞士公司帶來(lái)相當(dāng)大的銷售額。亞力兄制藥在獲批Kanuma和Strensiq之后,其上市產(chǎn)品的數(shù)量增加了兩倍,這標(biāo)志著該公司圍繞罕見(jiàn)病治療藥物建立的增長(zhǎng)模式將得到一個(gè)顯著的進(jìn)展。

分享到:









 相關(guān)新聞
相關(guān)新聞