一致性評價大幕開啟,醫院市場即將調整
2016年以來,CFDA陸續發布有關仿制藥一致性評價的相關政策和指導文件,5月26日, “總局關于落實《國務院辦公廳關于開展仿制藥質量和療效一致性評價的意見》有關事項的公告(2016年第106號)”發布,這也是近來CFDA最新的正式稿,隨著2018年底這個時限越來越近,監管部門和制藥企業都紛紛加快了一致性評價的步伐。
來源于基藥目錄,抗感染藥數量突出
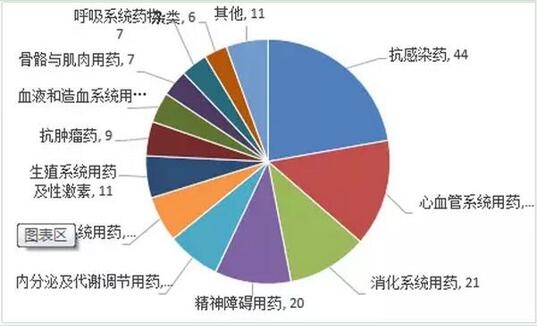
在《2018年底前須完成仿制藥一致性評價品種目錄》中,共涉及443個品規,253個產品,198個通用名。由于該目錄主要取自于2012版國家基本藥物的口服化藥,在治療領域分布上也有著類似的格局,抗感染藥在數量上保持絕對優勢,12版新增的口服抗腫瘤藥品種也全部入選該目錄。
圖1 、2018年底前須完成一致性評價品種的治療領域分布(以通用名計)氯吡格雷成目錄最大品種,市場集中度高
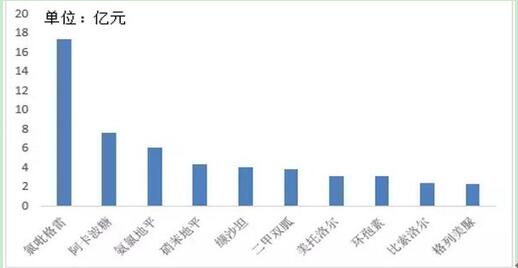
基于PDB國內樣本醫院市場數據,2015年,上述目錄品種占當年口服市場購藥金額的18.74%,且不乏用藥大品種(本次統計未考慮規格,僅以產品計,下同)。氯吡格雷遙遙領先于其他產品,也是唯一一個金額超過10億元的品種。隨后的9個產品里,糖尿病用藥占據3席(對應3種作用機制),高血壓用藥占據5席(對應3種作用機制),還有1個是免疫抑制劑,適應證集中度相當高。
圖2 、仿制藥一致性評價品種樣本醫院市場TOP10產品(2015年)
數據來源:中國醫藥工業信息中心藥物綜合數據庫PDB
跨國公司壓力不大,國內企業面臨嚴峻考驗
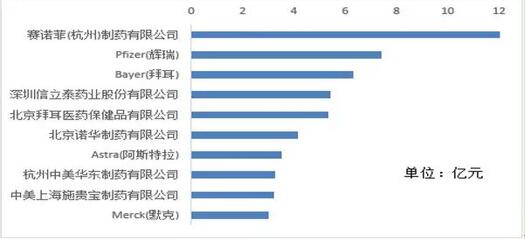
基于PDB國內樣本醫院市場數據,2015年,在上述目錄品種所對應的企業中,按照購藥金額排列,TOP10的企業幾乎都是跨國公司或合資公司,而此次一致性評價的范圍主要是“國產仿制藥、進口仿制藥和原研藥品地產化品種”,因此這些企業的壓力其實并不大;而唯一一家國內企業,深圳信立泰藥業股份有限公司,作為氯吡格雷的國內首仿企業,這次的一致性評價就顯得尤為重要,2015年,該品種占公司整體口服市場的97%以上。
圖3 、仿制藥一致性評價品種樣本醫院市場TOP10企業(2015年)
數據來源:中國醫藥工業信息中心藥物綜合數據庫PDB

分享到:








 相關新聞
相關新聞