



業務咨詢
中國:
Email: marketing@medicilon.com.cn
業務咨詢專線:400-780-8018
(僅限服務咨詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(781)535-1428(U.S.)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




近日,現代制藥連續發布了兩則公告,稱公司及全資子公司上海現代制藥海門有限公司收到CFDA核準簽發的《審批意見通知件》及《藥物臨床試驗批件》,共涉及兩個原料藥阿哌沙班和磷酸西格列汀以及它們的兩個片劑。數據顯示,阿哌沙班片和磷酸西格列汀片都屬于全球重磅產品,2016年在全球的銷售額均超過30億美元。目前,兩個產品都進入了新版醫保目錄,那么國內藥企誰能搶到首仿呢?
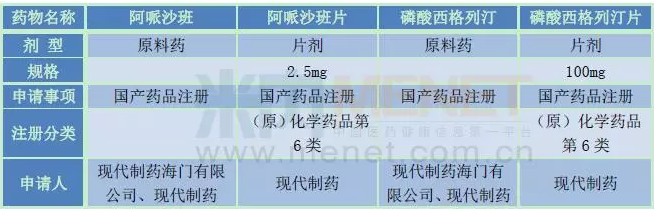
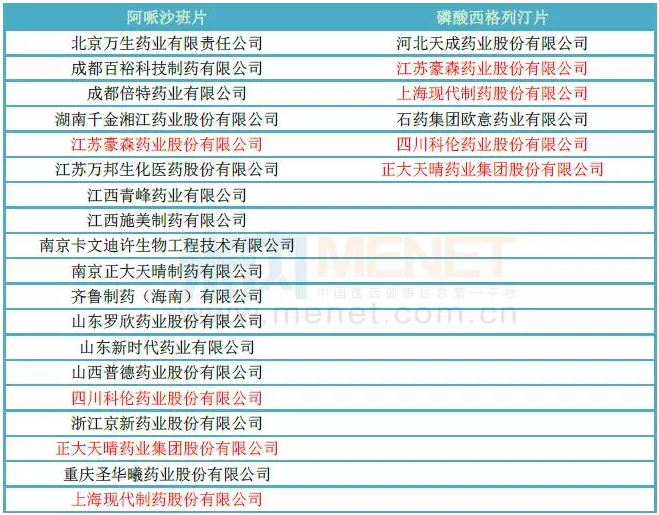
米內網數據顯示,目前國內已獲批臨床申請阿哌沙班片的企業有19家,而獲批臨床申請磷酸西格列汀片的企業有6家,其中上海現代制藥、江蘇豪森藥業、四川科倫藥業、正大天晴藥業均獲批了上述兩個產品。剔除重合的企業,目前這兩個產品已經有21個企業獲批了臨床,競爭如此之大,源于什么呢?
阿哌沙班是一種強效的、可逆的、高選擇性的Xa因子抑制劑,是新型口服抗凝藥物,能夠在不影響止血功能的劑量水平下發揮抗栓作用,可用于預防和治療血栓。臨床用于髖關節或膝關節擇期置換術的成年患者,預防靜脈血栓栓塞事件。
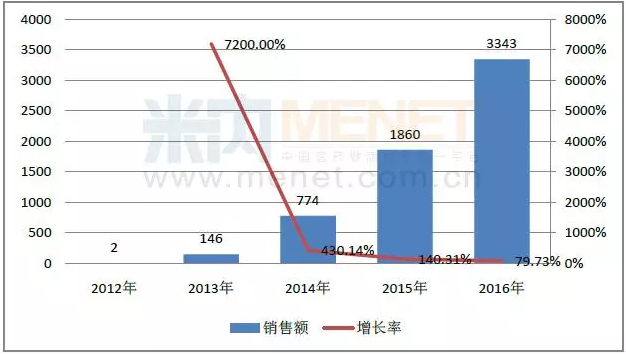
阿哌沙班由百時美施貴寶公司和輝瑞公司聯合研制開發,2011年在歐盟首次獲批上市,規格為2.5mg和5mg。米內網數據顯示,最近五年,阿哌沙班的全球銷售額在快速上漲,2015年突破10億美元關口,2016年更上漲至33.43億美元。
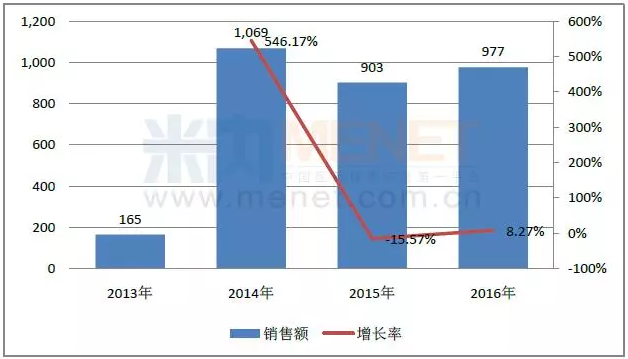
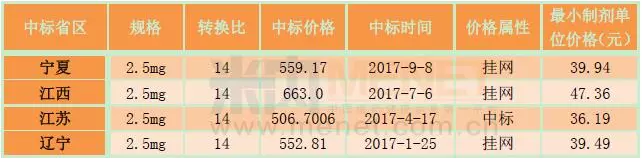
CFDA于2013年批準阿哌沙班在華上市,規格為2.5mg。數據顯示,2014-2016年間,阿哌沙班在中國城市公立醫院、縣級公立醫院、城市社區中心以及鄉鎮衛生院(簡稱中國公立醫療機構)終端的合計銷售額均保持在900萬-1000萬元左右。目前,阿哌沙班片已經進入了新版醫保目錄,是本次新增的乙類產品之一,使用范圍限下肢關節置換手術患者。
磷酸西格列汀為二肽基肽酶4(DPP-4)抑制劑類的口服降糖藥物,臨床上可單獨使用或與二甲雙胍聯用,用于治療2型糖尿病。磷酸西格列汀主要是通過增加活性腸促胰島激素的水平從而實現2型糖尿病患者對于血糖的控制。
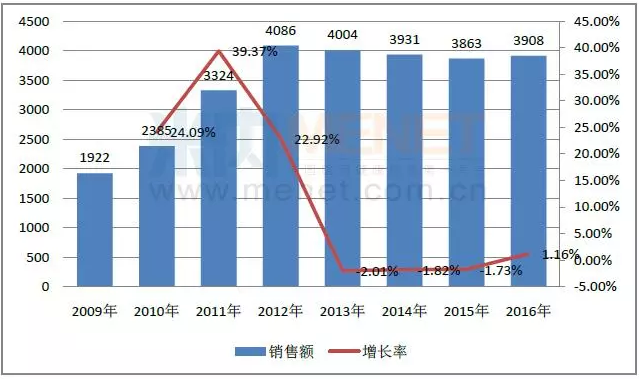
磷酸西格列汀由默克公司首先研制,最早于2006年10月在美國獲批上市。米內網數據顯示,磷酸西格列汀的全球銷售額在2012年到達了峰值,當年已經突破了40億美元,隨后幾年的銷售額出現了輕微下滑的現象,但仍保持在38億美元以上。
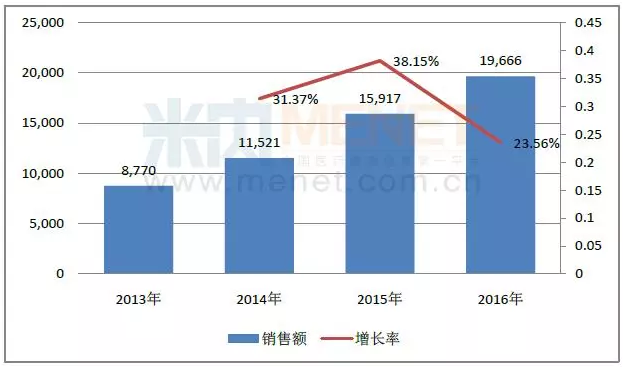
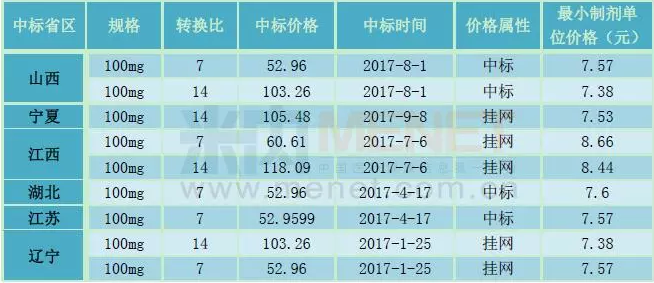
CFDA于2009年批準磷酸西格列汀片進入中國。米內網數據顯示,最近幾年,磷酸西格列汀片在中國公立醫療機構終端合計銷售額迅猛增長,每年的增長率保持在30%以上。在2016年中國公立醫療機構化學藥口服降血糖藥產品TOP20格局,磷酸西格列汀片排名第16位。目前,磷酸西格列汀片已經進入了新版醫保目錄,是本次新增的乙類產品之一,使用范圍限二線用藥。
從2016年的全球銷售情況來看,阿哌沙班片和磷酸西格列汀片都超過了30億美元,在抗凝以及降糖領域均已獲得不俗的成績。
阿哌沙班片進入中國市場的時間不長,但憑借其在全球市場的高速成長性,也吸引了眾多國內企業的垂青;磷酸西格列汀片雖然進入中國市場較早,市場份額已被默克公司牢牢緊握,但進了新醫保目錄后,國產產品的優勢將會得到展現,因此也有國內企業把目光盯緊在這里。
此外,自從實行了BE備案管理后,藥企也紛紛抓緊了這個大好機會。據媒體消息稱,江蘇豪森、正大天晴已完成了阿哌沙班片的BE試驗并提交了上市申請,而在登記的還有四川科倫、江蘇嘉逸、江蘇萬邦以及江西青峰等;四川科倫也完成了磷酸西格列汀片的BE試驗并提交仿制藥上市申請,目前登記的還有通化東寶、正大天晴以及浙江醫藥等。
每一場戰役都會有勝利者,這兩場首仿搶奪戰最終是何結局?我們一起拭目以待。
 相關新聞
相關新聞