



業務咨詢
中國:
Email: marketing@medicilon.com.cn
業務咨詢專線:400-780-8018
(僅限服務咨詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(781)535-1428(U.S.)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




單酰甘油酯酶(Monoacylglycerol lipase,MAGL)是一種絲氨酸水解酶[1],不僅能在脂質代謝中將三酰甘油分解為游離脂肪酸和甘油,為機體供能,而且能夠水解2-花生四烯酸甘油酯(2-AG),調節體內大麻素系統信號轉導。2-花生四烯酸甘油酯是內源性大麻素系統組成部分,而內源性大麻素與機體腦損傷保護,免疫應答,炎癥反應等有關;最新的研究指出,內源性大麻素系統在部分腫瘤中可以抑制癌細胞增殖,誘導腫瘤細胞凋亡,在腫瘤生長中影響腫瘤血管生成。
單酰甘油酯酶小百科
單酰甘油酯酶是絲氨酸水解酶家族中的一員,絲氨酸水解酶家族包括250種不同的蛋白酶,是原核和真核細胞中最龐大的酶家族之一。絲氨酸水解酶的激活是通過活性中心一組氨基酸殘基變化實現的,并在多種人體生理過程和疾病中起到關鍵作用,特別是在消化,凝血和補體系統方面。由于絲氨酸水解酶的重要研究價值使得大量的不同結構的絲氨酸水解酶抑制劑被研發出來,這些抑制劑一方面可作為潛在的治療藥物,另一方面可作為有價值的小分子探針來研究絲氨酸水解酶的功能。但是,盡管有多個先導結構被發現可以抑制絲氨酸水解酶,卻依舊缺乏高活性、高選擇性的抑制劑。
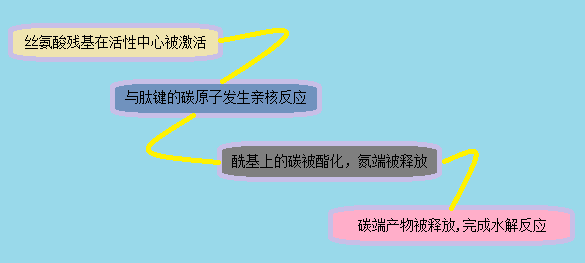
盡管絲氨酸水解酶在結構上存在高度差異性,但它們的催化機制卻是相同的,具體的過程是:
單酰甘油酯酶的體內調節作用
1,MAGL與脂質代謝網絡密切相關,MAGL可通過MAGL-FFA(游離脂肪酸)通路調節脂肪酸代謝網絡。
2,體內研究表明,MAGL的抑制劑在小鼠炎癥和神經性疼痛模型中發揮抑制大麻素Ⅰ型受體(CB1)的作用。
3,2012年,在阿爾茨海默氏病小鼠模型中證實:抑制MAGL能夠顯著降低淀粉樣神經病理,減少神經炎癥和退化,改善突觸和認知功能。
4,另外一些研究發現MAGL抑制劑對非甾體抗炎藥引起的胃出血模型和炎癥性腸病模型起到良性作用。
肝癌是常見的肝臟原發性惡性腫瘤,其致死率居世界第三位,并在世界范圍內呈現逐年上升趨勢。深入研究肝癌的發病機制,尋找肝癌組織中異常表達的基因或蛋白發現:肥胖和脂質代謝紊亂是肝癌發生的高危因素,而肥胖和脂質代謝紊亂又與單酰甘油酯酶密切相關。
MAGL在惡性黑色素瘤、乳腺癌及卵巢癌細胞中明顯升高,MAGs水平下降,游離脂肪酸(FFAs)水平上升。通過MAGL-FFA通路,惡性腫瘤細胞可以引起溶血磷脂酸(LPA)、溶血磷脂酰膽堿(LPC)、溶血磷脂酸乙醇胺(LPE)、前列腺素E2(PGE2)等一系列脂質信號分子水平上升。其中PGE2的上升,可使下游的Tyr397位點磷酸化,然后與蛋白受體和生長因子結合,促進細胞的轉移和侵襲能力。而溶血磷脂酸(LPA)能激活多種G蛋白偶聯受體,通過不同的抗凋亡信號通路,促進腫瘤細胞的存活和增殖。
部分已報道的MAGL抑制劑
在過去的10年里,一直在努力開發新型MAGL抑制劑,現已報道的小分子類MAGL抑制劑大約有20個,主要包括MAGL內源性底物2-AG的模擬類似物和各種從化合物庫中篩選獲得并改造的化合物。
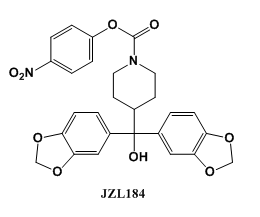
Long等[2]通過基于活性的蛋白譜學研究方法(activity-basedproteinprofiling,ABPP),發現哌啶氨基甲酸酯類化合物JZL184,其在低濃度下能選擇性抑制小鼠腦蛋白中MAGL的活性。在用JZL184處理小鼠后,2-花生四烯酸甘油酯(2-AG)的表達水平顯著提高5-10倍。
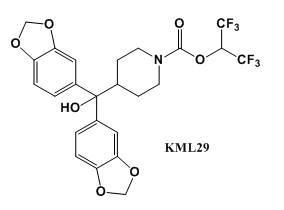
為了進一步的提高抑制劑的選擇性,Chang等[3]設計了化合物KML29,ABPP實驗表明KML29在活體及離體條件下均能選擇性抑制MAGL的活性。
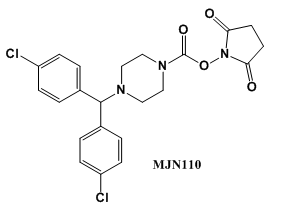
Niphakis等[4]發現丁二酰亞胺基甲酸酯類化合物MJN110,其同樣可以在活體及離體條件下高效、高選擇性抑制MAGL的活性。

2013年,Aaltonen等[5]發現哌啶三唑脲類化合物JJKK-048能超高效抑制MAGL的活性,其IC50值小于0.4Nm,同時在ABPP實驗發現:JJKK-048對MAGL具有極高的選擇性。
在小分子抑制劑不斷被研究開發過程中,天然產物一直以來都是其重要來源之一,已報道的天然MAGL抑制劑包括扁塑藤素,大戟二烯醇和丹參酮ⅡA3類結構,但是這三類結構均為萜類化合物,且都具有較高的親脂性,這限制了對這些化合物進一步進行藥物化學改造的可能性,因此尋找新型天然或非天然MAGL抑制劑仍是該研究領域的熱點。
MAGL抑制劑的近期研究熱點
盡管已經有多個MAGL抑制劑已經被報道,但是高活性、高選擇性、具有成藥性的MAGL抑制劑依舊卻乏。

單酰基甘油脂肪酶(MGLL或MAGL)是調節內源性大麻素和類二十醇類信號通路的一個臨界點,從而為神經和神經退行性疾病提供新的治療機會。Cisar等人在文獻[6]中提出了以六氟異丙基氨基甲酸酯為基礎的MGLL不可逆抑制劑的開發及優化,最終得到高效、選擇性和口服有效的ABX-1431。ABX-1431在一期臨床研究中耐受性良好,安全性高,并在患有神經系統疾病的患者中顯示了較好的初步結果。研究的數據表明,它是治療成人Gilles de la Tourette綜合癥的潛在藥物。ABX-1431目前已經成功地完成了一期臨床試驗,正進入神經障礙的臨床研究的第二階段,并對其他適應癥,如視神經鞘炎和多發性硬化進行臨床試驗。
ABX-1431的合成路線:
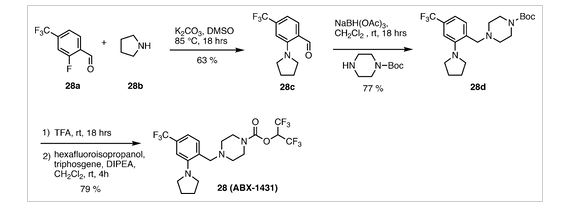
在Jumpei Aida等人[7]近期發表的文獻中,以哌嗪吡咯啶化合物2b為基礎,通過改進設計,增強哌嗪吡咯啶核及其取代基與MAGL酶的相互作用,找到了一種有效且可逆的MAGL抑制劑化合物(R)-3t。在給小鼠口服(R)-3t后,可升高小鼠的2-花生四烯酸甘油酯(2-AG)水平。由此可見(R)-3t是一種可能成藥的單酰甘油酯酶的小分子抑制劑,值得進一步的探究。

MAGL不可逆轉的抑制劑在重復給藥后會使小鼠產生交叉耐受性。慢性MAGL阻滯還會引起生理依賴,損害內源性大麻素突觸可塑性。而可逆的MAGL抑制劑可以抑制酶活性的同時保持endocan-nabinoid系統完整。在這些問題基礎上,可逆抑制劑的應用可能會是MAGL抑制劑領域的一個重要發展。
參考文獻:
1,Gil-Ordonez, A. Martin-Fontecha, M. Ortega-Gutierrez, S. Lopez-Rodriguez, M. L.Monoacylglycerol lipase (MAGL) as a promising therapeutic target. Biochem.Pharmacol. 2018.
2,Long J Z, Li W, Booker L et al. Selective blockade of 2-arachidonoylglycerolhydrolysis produces cannabionoid behavioral effects. Nature Chemical Biology,2009,5 (1):37-44.
3,Chang JW1, Niphakis MJ, Lum KM et al. Highly selective inhibitors ofmonoacylglycerol lipase bearing a reactive group that is bioisosteric withendocannabinoid substrates. Chem Biol. 2012 May 25;9(5):579-88.
4,Niphakis MJ, Cognetta AB, Chang JW et al. Evaluation of NHS carbamates as apotent and selective class of endocannabinoid hydrolase inhibitors. ACS ChemNeurosci. 2013 Sep 18;4(9):1322-32.
5,Aaltonen N1, Savinainen JR, Ribas CR et al. Piperazine and piperidine triazoleureas as ultrapotent and highly selective inhibitors of monoacylglycerollipase. Chem Biol. 2013 Mar 21;20(3):379-90.
6,Justin S. Cisar, Olivia D. Weber, Jason R. Clapper et al. Ezekowitz, Gary P.O’Neill?, and Cheryl A. Grice. Identification of ABX-1431, a SelectiveInhibitor of Monoacylglycerol Lipase and Clinical Candidate for Treatment ofNeurological Disorders. J. Med. Chem. 2018, 61, 20, 9062-9084.
7,JumpeiAida, Makoto Fushimi, Tomokazu Kusumoto et al. Design, Synthesis, andEvaluation of Piperazinyl Pyrrolidin-2-ones as a Novel Series of ReversibleMonoacylglycerol Lipase Inhibitors. J. Med. Chem. 2018, 61, 20, 9205-9217.
 相關新聞
相關新聞