



業(yè)務(wù)咨詢
中國:
Email: marketing@medicilon.com.cn
業(yè)務(wù)咨詢專線:400-780-8018
(僅限服務(wù)咨詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(781)535-1428(U.S.)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




HIV是一種會(huì)攻擊人體免疫系統(tǒng)的病毒,主要攻擊目標(biāo)是人體免疫系統(tǒng)中最重要的CD4T淋巴細(xì)胞,并大量破壞該細(xì)胞,使人體逐漸喪失免疫功能,從而導(dǎo)致人體易于感染各種疾病,甚至發(fā)生惡性腫瘤,且病死率較高。目前,全球約有3670萬艾滋病病毒感染者,每年大約有110萬人死于艾滋病,而新發(fā)感染者大約每年有210萬。
作為G蛋白偶聯(lián)因子超家族(GPCR)成員的細(xì)胞膜蛋白,趨化因子受體CCR5是HIV-1入侵機(jī)體細(xì)胞的主要輔助受體。CCR5抑制劑藥物與CCR5結(jié)合后,使CCR5構(gòu)象發(fā)生變化,阻斷了HIV-1與細(xì)胞膜蛋白結(jié)合,導(dǎo)致HIV-1與CCR5在細(xì)胞表面結(jié)合的數(shù)量減少,從而起到抗感染作用。因此,CCR5可視為抗HIV-1藥物的篩選靶點(diǎn),值得廣泛關(guān)注并進(jìn)行細(xì)致研究。
關(guān)于AIDS和CCR5 的小百科
人類獲得性免疫缺陷綜合征(簡稱艾滋病,AIDS)在1981年被首次發(fā)現(xiàn),25年以來,作為人類歷史上最致命的流行病之一,HIV一度被認(rèn)為是死刑。隨著研究發(fā)展,AIDS已經(jīng)成為一種可控制的疾病,但是仍無有效治愈手段。
趨化因子是一類具有趨化活性的小分子細(xì)胞因子,屬于G蛋白偶聯(lián)受體家族。它的功能在于使細(xì)胞表面具有跨膜G蛋白偶聯(lián)受體的細(xì)胞聚集在一起,參與體內(nèi)的免疫平衡作用。趨化因子受體CCR5,是人體細(xì)胞表面的一種蛋白受體。早在1996年,科學(xué)家就發(fā)現(xiàn),CCR5和另一種蛋白CXCR4是艾滋病病毒HIV-1進(jìn)入人體細(xì)胞的主要入點(diǎn)。其中,利用CCR5侵入細(xì)胞的病毒株稱為R5嗜性,利用CXC4侵入的稱為X4嗜性。不同的感染時(shí)期,HIV的嗜性也有變化,一般在感染初期為R5嗜性,隨著感染的加深向X4嗜性轉(zhuǎn)化。
CCR5是由352個(gè)氨基酸組成,在結(jié)構(gòu)上分為胞外N端,3個(gè)胞外環(huán),三個(gè)胞內(nèi)環(huán),7個(gè)跨膜α螺旋和胞內(nèi)C端,其同源配體包括CCL3、CCL4和CCL3L1。CCR5是細(xì)胞內(nèi)β趨化因子(RANTES、MIP1α和MIP1β)的受體,具有調(diào)控T細(xì)胞和單核細(xì)胞、巨嗜細(xì)胞的遷移、增殖與免疫的功能,主要表達(dá)在T細(xì)胞,巨噬細(xì)胞、樹突狀細(xì)胞、嗜酸性粒細(xì)胞、小膠質(zhì)細(xì)胞和乳腺或前列腺癌細(xì)胞的族群中[1]。
CCR5在HIV侵入人體過程中扮演的角色
HIV分為HIV-1和HIV-2兩種亞型,HIV-1致病力強(qiáng),人類獲得性免疫缺乏癥(AIDS)主要是由于被HIV-1病毒感染,其能在體內(nèi)快速繁殖而導(dǎo)致宿主免疫細(xì)胞的大量破壞所致。在 HIV-1 進(jìn)入白細(xì)胞過程中,結(jié)構(gòu)正常的 CCR5 蛋白質(zhì)起到促進(jìn) HIV-1入胞的通道蛋白的功能。

HIV-1進(jìn)入靶細(xì)胞內(nèi)部,導(dǎo)致細(xì)胞損壞死亡,從而降低機(jī)體的免疫力是一個(gè)復(fù)雜的過程:
在HIV-1侵入靶細(xì)胞時(shí),首先會(huì)發(fā)生的是病毒表面的囊膜蛋白gp120與靶細(xì)胞表面的CD4+ T分子相互作用,致使gp120的V3可變環(huán)區(qū)暴露。
隨后在趨化因子受體CCR5或CXCR4的進(jìn)一步的協(xié)助下,受體N-末端的酪氨酸和其它一些酸性的氨基酸會(huì)相應(yīng)的黏附到gp120蛋白暴露的V3區(qū)上,與病毒的gp120/CD4形成復(fù)合體。
接下來,病毒的跨膜蛋白gp41會(huì)發(fā)生一系列的構(gòu)象變化,其自身會(huì)形成螺旋六聚體結(jié)構(gòu),促使gp41蛋白分子的N端疏水區(qū)向著胞膜方向移動(dòng),進(jìn)而與靶細(xì)胞融合。
當(dāng)HIV-1成功與靶細(xì)胞融合后會(huì)導(dǎo)致細(xì)胞死亡和被破壞,而HIV-1病毒會(huì)從細(xì)胞內(nèi)出來,再次通過其他CD4+ T細(xì)胞上的CCR5受體進(jìn)入其他正常的細(xì)胞。這樣周而復(fù)始,就使體內(nèi)CD4+ T免疫細(xì)胞的數(shù)量越來越少,機(jī)體的免疫力也逐漸下降,逐漸發(fā)展成為艾滋病,并出現(xiàn)很多的機(jī)會(huì)感染或生成腫瘤,從而致使人體死亡。
由于HIV-1病毒在與靶細(xì)胞結(jié)合后會(huì)使得人體的免疫力降低,使得人體有更多的可能性會(huì)感染腫瘤,因此阻斷CCL5-CCR5通路會(huì)起到一定的抗腫瘤作用,其兩個(gè)抗腫瘤機(jī)制分別是:
機(jī)制1:促進(jìn)巨噬細(xì)胞M2亞型到M1型轉(zhuǎn)換。一般在腫瘤組織周圍會(huì)有很多巨噬細(xì)胞浸潤,這些大量的腫瘤相關(guān)巨噬細(xì)胞(TAM)也叫M2型巨噬細(xì)胞,它們通常沒有殺傷腫瘤細(xì)胞的作用,反而會(huì)釋放很多趨化因子和細(xì)胞因子促進(jìn)腫瘤生長和轉(zhuǎn)移。當(dāng)CCR5抑制劑阻斷CCL5-CCR5通路后,M2型促進(jìn)腫瘤生長的巨噬細(xì)胞就會(huì)轉(zhuǎn)化成具有一定殺傷腫瘤細(xì)胞能力的M1型巨噬細(xì)胞。
機(jī)制2:免疫調(diào)節(jié)和改變腫瘤周圍的炎性微環(huán)境。CCR5抑制劑盡管不會(huì)直接殺傷腫瘤細(xì)胞,但阻斷CCR5通路后,刺激腫瘤生長的趨化因子和細(xì)胞因子都會(huì)下調(diào),腫瘤周圍的炎性微環(huán)境也會(huì)改善;同時(shí),腫瘤周圍的保護(hù)性間質(zhì)會(huì)減少,表皮向間質(zhì)轉(zhuǎn)化能力也會(huì)下降。這種對腫瘤周圍環(huán)境的影響,可以幫助免疫檢查點(diǎn)抑制劑或化療藥物更好地殺滅腫瘤細(xì)胞。
趨化因子受體CCR5在病毒感染靶細(xì)胞過程中起到非常關(guān)鍵的作用,而在一些發(fā)生CCR5突變的人群中,CCR5的基因序列缺失突變,第185個(gè)氨基酸后的32個(gè)氨基酸全部缺失,這導(dǎo)致CCR5不能正常表達(dá)于細(xì)胞表面,從而可以阻滯HIV的侵入,使得CCR5突變的人群會(huì)對HIV病毒有免疫作用。由此可見,阻斷該受體的功能是一個(gè)新穎、合理的治療HIV手段。
已報(bào)道的CCR5抑制劑總結(jié)
病毒入侵過程是一個(gè)級聯(lián)的結(jié)合與構(gòu)象變化反應(yīng),根據(jù)病毒入侵復(fù)制裂解的不同階段,拮抗劑可分為病毒入侵拮抗劑(如CD4拮抗劑、輔助受體拮抗劑)、逆轉(zhuǎn)錄酶拮抗劑、融合拮抗劑、整合酶拮抗劑、蛋白酶抑制劑等。目前得到美國食品與藥品監(jiān)督管理局(FDA)批準(zhǔn)的抗HIV-1藥物已有30多種,其中17種是逆轉(zhuǎn)錄酶抑制劑(包括13種核苷類逆轉(zhuǎn)錄酶抑制劑及4種非核苷類逆轉(zhuǎn)錄酶抑制劑),11種蛋白酶抑制劑,1種CCR5受體抑制劑(maraviroc),1種整合酶抑制劑(raltegravir)以及1種融合抑制劑(T20)。
雖然已經(jīng)有了很多種HIV抑制劑的研發(fā)上市,但卻仍未發(fā)現(xiàn)一種治療艾滋病的特效藥。雞尾酒療法,是在1996年由美籍華裔科學(xué)家何大一提出,是通過三種或三種以上的抗病毒藥物聯(lián)合使用來治療艾滋病。該療法的應(yīng)用可以減少單一用藥產(chǎn)生的抗藥性,最大限度地抑制病毒的復(fù)制,使被破壞的機(jī)體免疫功能部分甚至全部恢復(fù),從而延緩病程進(jìn)展,延長患者生命,提高生活質(zhì)量。
在HIV抑制劑中,病毒入侵拮抗劑中的CCR5抑制劑受到廣泛的關(guān)注。其作為抗HIV-1病毒感染的靶點(diǎn),主要是基于其兩方面的作用:一是通過阻斷CCR5與gp120之間的相互作用阻斷病毒的感染;二是通過降低或敲除靶細(xì)胞表面CCR5的表達(dá)量,進(jìn)而阻斷病毒的感染。以CCR5為靶點(diǎn)的HIV-1受體拮抗劑越來越受關(guān)注,主要有趨化因子衍生物、非肽類小分子化合物、單克隆抗體、肽類化合物等4類。目前已有幾種CCR5抑制劑正處于臨床前和臨床試驗(yàn)中。
1,已上市的CCR5拮抗劑Maraviroc。Maraviroc的作用機(jī)制是能夠占據(jù)病毒囊膜蛋白gp120與CCR5的結(jié)合位點(diǎn),使得病毒與CCR5直接作用的機(jī)率降低,可以有效的抑制病毒與該受體的結(jié)合。Maraviroc的細(xì)胞毒性研究發(fā)現(xiàn)無不良影響,對CCR5具有高度選擇性,在2007年8月被美國FDA批準(zhǔn)用于臨床治療艾滋病。
2,在研臨床階段的CCR5小分子抑制劑。化學(xué)小分子抑制劑因其不具有炎癥應(yīng)答效應(yīng),且生產(chǎn)成本低等原因,在CCR5抑制劑的研究中占據(jù)了主要的地位。十幾年來,在投入了大量的科研成本后,合成了幾十種小分子CCR5抑制劑,其中已進(jìn)入臨床試驗(yàn)研究的有下列幾個(gè)。

Maraviroc的成功,推動(dòng)了CCR5抑制劑的研究進(jìn)展,目前在臨床Ⅱ期試驗(yàn)中的CCR5抑制劑Cenicriviroc,具有良好抗病毒效果。Cenicriviroc不僅可以結(jié)合CCR5,還可以抑制CCR2,使HIV感染者的免疫和代謝等功能增強(qiáng)。
CCR5抑制劑最新研究進(jìn)展
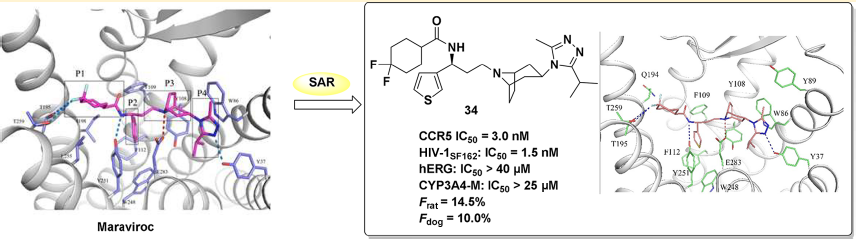
CCR5受體是一個(gè)具有較大吸引力的目標(biāo),Maraviroc是唯一已上市的CCR5抑制劑。PanfengPeng[2]等人克服maraviroc的缺點(diǎn),設(shè)計(jì)、合成并測試了一個(gè)新型CCR5抑制劑--小分子化合物34,其能提高抗艾滋病效力和生物利用度。
小分子化合物34是最有活性的CCR5抑制劑,有優(yōu)良的體外抑制HIV-1的活性,且其細(xì)胞毒性低,藥效動(dòng)力學(xué)優(yōu)秀。因此,化合物34是一種有前景的能夠治療艾滋病毒感染的候選藥物,值得進(jìn)一步的研究和測試。
參考文獻(xiàn):
1, Sicoli D, JiaoX, Ju X, et al. CCR5 receptor antagonists block metastasis to bone of v-Srconcogene-transformed metastatic prostate cancer cell lines. Cancer Research.2014, 74 (23): 7103-14.
2, Panfeng Peng,Huan Chen, et al. Structure-Based Design of 1 Heteroaryl-1,3-propanediamineDerivatives as a Novel Series of CC-Chemokine Receptor 5 Antagonists. J. Med.Chem. 2018, 61, 9621-9636.
 相關(guān)新聞
相關(guān)新聞