前列腺癌是男性中常見的惡性腫瘤,開發(fā)用于治療前列腺癌的有效療法一直是科學(xué)研究的主要焦點。前列腺是一種雄激素依賴性器官,前列腺癌是一種雄激素依賴性疾病。雄激素作用由雄激素受體 (AR) 介導(dǎo),AR 是一種激素激活的轉(zhuǎn)錄因子,AR 屬于核受體超家族中的類固醇受體。AR 及其下游信號傳導(dǎo)在局部和轉(zhuǎn)移性前列腺癌的發(fā)展和進展中起關(guān)鍵作用。
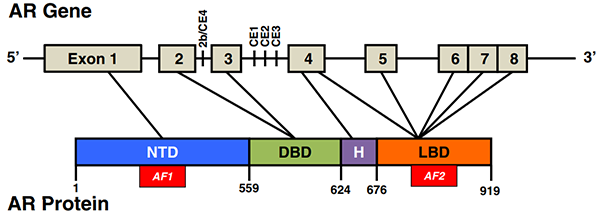
雄激素受體(AR)結(jié)構(gòu)[1]
轉(zhuǎn)移性前列腺癌的主要治療方法是雄激素剝奪療法 (ADT)。許多靶向 AR 的藥物已被開發(fā)用于治療晚期前列腺癌,包括阻斷雄激素合成的 Abiraterone,及與 AR 結(jié)合的 AR 拮抗劑 Enzalutamide、Apalutamide 和 Darolutamide。但這些藥物通常在治療后 2 年內(nèi)出現(xiàn)耐藥。在大多數(shù)對 AR 拮抗劑耐藥的腫瘤中,AR 信號繼續(xù)發(fā)揮作用并驅(qū)動腫瘤生長和進展。去勢抵抗性前列腺癌 (CRPC) 依賴于 AR。AR 基因擴增、點突變和選擇性剪接已被確定為對這些靶向 AR 的藥物產(chǎn)生耐藥性的一些主要機制。此外,類固醇代謝、細胞信號和輔助調(diào)節(jié)蛋白的變化也是 CRPC 中 AR 再激活的重要因素。大多數(shù) AR 靶向治療都針對激素結(jié)合域。缺乏激素結(jié)合結(jié)構(gòu)域的組成型活性 AR 剪接變體經(jīng)常在 CRPC 中表達,這一發(fā)現(xiàn)強調(diào)了開發(fā)針對 AR 其他部分的療法的必要性。所以,迫切需要開發(fā)針對 AR 治療前列腺癌的新治療策略,特別是針對轉(zhuǎn)移性去勢抵抗性前列腺癌 (mCRPC)。mCRPC 到目前為止仍然無法治愈且致命。
靶向降解雄激素受體 (AR)
AR 蛋白的誘導(dǎo)降解在靶向 AR 信號傳導(dǎo)方面可能比傳統(tǒng)的 AR 拮抗劑更有效。選擇性雄激素受體降解劑 (SARD) 與 AR 中的配體結(jié)合結(jié)構(gòu)域結(jié)合并破壞 AR 與輔助調(diào)節(jié)劑的相互作用,導(dǎo)致蛋白酶體依賴性 AR 降解。另一種實現(xiàn)誘導(dǎo) AR 降解的新策略是基于蛋白水解靶向嵌合體 (PROTAC) 技術(shù)平臺。基于
PROTAC 的 AR 降解劑是一種雙功能小分子,由與 AR 蛋白結(jié)合的 AR 配體和與 E3 連接酶復(fù)合物結(jié)合并通過 Linker 連接在一起的配體組成。PROTAC 小分子降解劑已成為一種很有前途的新型治療劑,但設(shè)計具有優(yōu)異口服
藥代動力學(xué)的 PROTAC 降解劑是一項重大挑戰(zhàn)。在一些研究中,科研人員根據(jù)新的策略,設(shè)計合成了具有較高口服生物利用度的的高效 PROTAC AR 降解劑。
PROTAC AR 降解劑 ARD-2128
下文中科研人員使用 Thalidomide 募集 Cereblon/cullin 4A E3 連接酶并通過 Linker 進行固化,在小鼠中發(fā)現(xiàn)了具有良好口服藥代動力學(xué)特性的高效 AR 降解劑 ARD-2128。

在此項研究中,科研人員通過
美迪西評估了五種高效 AR 降解劑在小鼠中靜脈和口服給藥的藥代動力學(xué) (PK) 數(shù)據(jù),其中最優(yōu)化合物為 ARD-2128。PK 數(shù)據(jù)顯示,ARD-2128 具有出色的整體 PK 曲線:低清除率 (1.2 mL/min/kg) 和中高穩(wěn)態(tài)分布容積 (V
ss 為2.7 L/kg)。ARD-2128 按 2 mg/kg 劑量靜脈給藥后的 T
1/2 為 27.6 小時,按 5 mg/kg 劑量口服給藥后 T
1/2 為 18.8 小時。ARD-2128 (5 mg/kg) 在小鼠體內(nèi)達到 67% 的口服生物利用度,通過口服給藥有效降低 AR 蛋白并抑制腫瘤組織中的 AR 調(diào)節(jié)基因,從而有效抑制小鼠腫瘤生長且無毒性跡象。
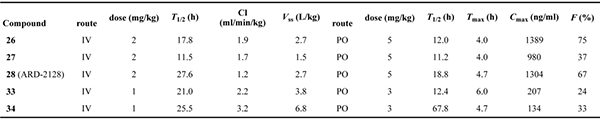
五種化合物在雄性 ICR 小鼠中的 PK 數(shù)據(jù)匯總[2]
此外,科研人員通過美迪西測試了 ARD-2128 在小鼠、大鼠、犬、猴和人五種屬中的血漿穩(wěn)定性。數(shù)據(jù)顯示,ARD-2128 在所有五種屬中都具有穩(wěn)定的血漿穩(wěn)定性。

ARD-2128 在五種屬中的血漿穩(wěn)定性[2]
PROTAC AR降解劑 ARD-2585
下文中科研人員報道了一些高效且具有口服生物利用度的 PROTAC AR 降解劑,其中 ARD-2585 是最有潛力的一個。ARD-2585 是一種口服有效的 PROTAC AR 降解劑。ARD-2585 在具有 AR 基因擴增的 VCaP 細胞系和攜帶 AR 突變的 LNCaP 細胞系中 DC50 值達到 ≤0.1 nM 。ARD-2585 有效抑制 VCaP 和 LNCaP 細胞生長,IC50 值分別為 1.5 和 16.2 nM,并在小鼠中具有出色的藥代動力學(xué)和口服生物利用度 (51%)。ARD-2585 在抑制 VCaP 腫瘤生長方面比 Enzalutamide 更有效,且不會對小鼠造成任何毒性跡象。所以,ARD-2585 是一種有前途的 AR 降解劑,可用于治療晚期前列腺癌。

科研人員研究了 ARD-2585 在 VCaP 和 LNCaP 細胞系中誘導(dǎo) AR 降解的作用機制,發(fā)現(xiàn)處理 3 小時后,ARD-2585 (100 nM) 可有效降低 VCaP 和 LNCaP 細胞中的 AR 蛋白。使用 AR 抑制劑、Cereblon 配體 Thalidomide、蛋白酶體抑制劑 MG-132 和 E1 Neddylation 抑制劑 MLN4924 預(yù)處理,有效阻斷 AR 降解。這些數(shù)據(jù)提供了明確的機制證據(jù),表明 ARD-2585 通過 Cereblon、蛋白酶體和 neddylation 依賴性機制誘導(dǎo) AR 降解,因此是真正的 PROTAC AR 降解劑。
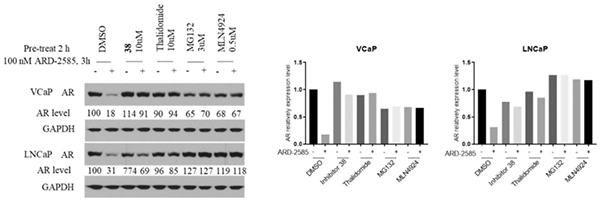
ARD-2585 的作用機制[3]
科研人員接下來測試了 ARD-2585 在 VCaP 異種移植腫瘤模型中的抗腫瘤活性,對照組為 Enzalutamide。ARD-2585 按 10、20 和 40 mg/kg 三種劑量給藥均有效抑制腫瘤生長。在治療結(jié)束時 (第 37 天),與空白對照組相比,ARD-2585 抑制腫瘤生長分別達54.9%、74.3% 和 65.9%。相比之下,Enzalutamide (40 mg/kg) 抑制腫瘤生長為 45.0%。所以,ARD-2585 (20 和 40 mg/kg)在抑制腫瘤生長方面比 40 mg/kg 的 Enzalutamide 更有效。同時,ARD-2585 和 Enzalutamide 均具有良好的耐受性,且在整個實驗期間均未引起動物體重減輕或其他毒性跡象。
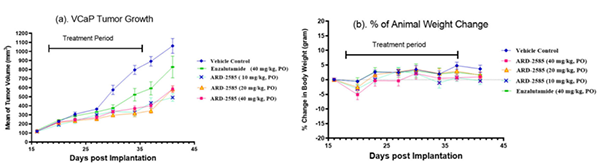
ARD-2585 在 VCaP 異種移植腫瘤模型中的功效[3]
藥效學(xué) (PD) 數(shù)據(jù)還顯示,對攜帶 VCaP 異種移植腫瘤的小鼠單次口服給藥 ARD-2585 (20 mg/kg)。腫瘤組織的 Western 分析顯示,ARD-2585 在 6 和 24 小時能有效降低 AR 蛋白水平,在 24 小時作用更強。
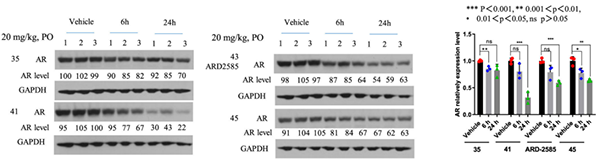
AR 降解劑對 VCaP 腫瘤中 AR 蛋白的藥效學(xué) (PD)作用[3]
科研人員評估了ARD-2585在小鼠中靜脈和口服給藥的藥代動力學(xué) (PK)數(shù)據(jù),ARD-2585 按 2 mg/kg 的劑量靜脈給藥后,具有優(yōu)異的分布容積 (Vss=1.8 L/kg)、長半衰期 (T1/2=5.5 h) 、及低清除率 (Cl=0.3 L/h/kg)。ARD-2585 按 5 mg/kg的劑量口服給藥后,Cmax 達到 1140 ng/mL。AUC 達到 8254 h*ng/mL,口服生物利用度為 51%。
最后科研人員通過美迪西對 ARD-2585 進行了全面的代謝測定,包括 ARD-2585 在肝微粒體中的代謝穩(wěn)定性、血漿穩(wěn)定性、及 hERG 實驗。證實 ARD-2585 在五種不同種屬 (小鼠、大鼠、犬、猴和人)具有穩(wěn)定的肝微粒體中的代謝穩(wěn)定性和血漿穩(wěn)定性。T
1/2>120 分鐘。人 ERG (人 ether-à-go-go相關(guān)基因)通道的體外抑制已被用作評估藥物分子潛在心臟毒性的重要試驗。科研人員通過美迪西進行了
hERG 實驗。測試 ARD-2585 對在 HEK 293 細胞系中穩(wěn)定表達的 hERG 鉀通道電流的體外影響,使用膜片鉗技術(shù)來確定 ARD-2585 對 hERG 電流抑制的濃度-反應(yīng)關(guān)系。發(fā)現(xiàn) ARD-2585 在高達 30 μM (測試的最高濃度) 下對 hERG 沒有抑制作用。
結(jié)語
以上研究可用于治療前列腺癌的口服活性 PROTAC AR 降解劑的開發(fā),并為口服活性 PROTAC 降解劑的設(shè)計提供見解和指導(dǎo)。兩項研究都借助了美迪西 PROTAC 藥物發(fā)現(xiàn)技術(shù)平臺和臨床前 DMPK 評價體系。美迪西 PROTAC 藥物發(fā)現(xiàn)技術(shù)平臺不僅包含設(shè)計合成 PROTAC-POI 和進行 PROTAC-POI 的體外篩選,還能對 PROTAC-POI 進行動物體內(nèi)藥效檢測和 PK/PD 研究、藥學(xué)分析、藥物代謝動力學(xué)研究和安全性評價,并匯總實驗結(jié)果和材料進行
IND 申報,以助力客戶加快 PROTAC-POI 藥物的研發(fā)進程。
參考文獻:
[1]. AyeshaA Shafi, et al. Androgen receptors in hormone-dependent and castration-resistantprostate cancer. PharmacolTher. 2013 Dec;140(3):223-38.
[2]. Xin Han, et al. Strategies toward Discovery of Potent and Orally Bioavailable ProteolysisTargeting Chimera Degraders of Androgen Receptor for the Treatment of ProstateCancer. J Med Chem. 2021 Sep9;64(17):12831-12854.
[3]. Weiguo Xiang, et al. Discovery of ARD-2585 as an Exceptionally Potent and Orally Active PROTACDegrader of Androgen Receptor for the Treatment of Advanced Prostate Cancer. J Med Chem. 2021 Sep 23;64(18):13487-13509.
美迪西PROTAC藥物臨床前DMPK評價體系
美迪西 DMPK 團隊,通過 PROTAC 技術(shù)原理,結(jié)合研發(fā)案例,利用完善的
體外 ADME、
體內(nèi) PK測試平臺,在小分子化合物研究基礎(chǔ)上,建立起一套關(guān)于 PROTAC 藥物的篩選和 IND 評價體系,關(guān)注藥物的溶解度、滲透性、代謝穩(wěn)定性、代謝產(chǎn)物鑒定與體內(nèi) PK 研究等,幫助客戶快速推進 PROTAC 藥物的研發(fā)。


聯(lián)系我們:
電話: +86 (21) 5859-1500(總機)
















 相關(guān)新聞
相關(guān)新聞