



業務咨詢
中國:
Email: marketing@medicilon.com.cn
業務咨詢專線:400-780-8018
(僅限服務咨詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(781)535-1428(U.S.)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com





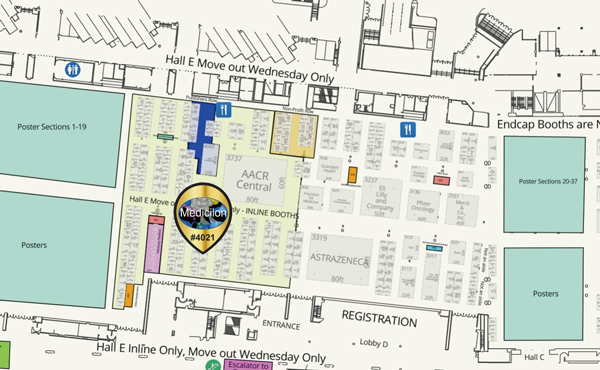
2024年4月5-10日,美國癌癥研究協會(AACR)年會將于在美國圣地亞哥舉行。AACR成立于1907年,是成立最早、規模最大的癌癥研究學會之一,致力于進行全面、創新和高水準癌癥研究。作為全球癌癥新藥研發的風向標,AACR聚集了高質量的腫瘤早期研究和創新進展,尤其會發布大量的創新靶發現、臨床前研究數據和早期臨床研究結果。美迪西執行副總裁兼美國公司總裁林慶聰博士將帶領美迪西美國團隊出席此次大會,我們在展位4021等您!


作為國內較早為客戶提供臨床前動物實驗的CRO公司之一,美迪西具備全面的臨床前研究服務能力,能夠提供系統的體內藥效學、藥代動力學和GLP安全性評價研究服務。目前美迪西已擁有多種穩定的藥效評價模型,可對細胞毒及靶向類小分子、單抗及雙特異抗體等大分子藥物、ADC、CAR-T/CAR-NK細胞治療抗腫瘤新藥提供全面系統的評價。美迪西對大量化學藥物和生物藥物建立了系統分析方法和體內外評價方法,包括小分子和大分子生物分析平臺、免疫分析工作站及放射性同位素藥代動力學研究平臺等,支持早期篩選、成藥性評價和IND申報等。
美迪西擁有經中國NMPA認證的GLP資質,且通過了美國FDA的GLP現場檢查,具備符合國際標準的GLP體系,并且獲得AAALAC認證,實驗動物管理質量標準獲得國際認可。至2023年底,美迪西已為全球2000+客戶提供藥物研發服務,參與研發完成的新藥及仿制藥項目已有421件IND獲批臨床,與國內外優質客戶共同成長。
經過20年的沉淀積累,藥效部已建立~400腫瘤藥效評價模型(包括PDX模型、同種腫瘤移植模型、異種腫瘤移植模型、人源化腫瘤移植模型等);~230非腫瘤疾病藥效評價模型,其領域涵蓋了神經精神系統、心腦血管系統、消化系統、炎癥免疫系統、內分泌及代謝系統、眼科及其他等熱點疾病領域。
藥效部門具備擁有深厚專業理論知識和多年實驗經驗的專業團隊,具備全面評價各種類別新藥藥效的大部分先進實驗設施,可從分子水平、細胞水平、ex-vivo、in vivo的多層次,全面評價從成藥性到一類創新藥的各種類型新藥的藥理藥效。可對小分子化藥、ADC藥物、細胞制劑、單抗、中藥等多種類別的藥物進行臨床前的系統藥效評價(包括口服制劑、注射劑、局部外用制劑、滴鼻劑、噴霧劑等),為新藥申報提供全面真實的試驗資料及研究報告。至今已受到眾多業內客戶的高度認可。

林慶聰,美國紐約愛因斯坦醫學院分子細胞生物學博士,曾連續四年榮獲“SAPA-NE服務獎”,獲評“北京海外人才”、“南京大學優秀青年教師”等榮譽稱號。林博士學術背景深厚,曾在美國阿爾伯特·愛因斯坦醫學院Raju Kucherlapati’s實驗室、哈佛大學醫學院從事分子遺傳學研究等,曾任哈佛大學醫學院遺傳和基因組學研究中心基因工程實驗室總監,在MCB、JBC等國際權威期刊上發表24篇論文,并榮獲多項發明專利。多年學術浸潤,使他在細胞生物學、分子生物學、免疫學、藥理學、抗體藥物發現和開發、發育生物學、生物信息學以及功能遺傳學和基因組學等領域沉淀了極高的學術造詣和扎實的技術功底。
深耕生物醫藥研發領域近40載,林博士不僅在學術界產生了重要影響,也為全球生物醫藥行業的發展做出了卓越貢獻,曾為跨國公司締造子公司,組建多個科學團隊,領導百余個藥物項目研發,在細胞生物學、分子遺傳學、基因工程的腫瘤小鼠模型研究與應用領域頗有研究,在抗體藥物研發、雜交瘤細胞抗體和人噬菌體抗體庫的建立、抗體基因工程、抗體人源化和親和力提高與成熟,以及哺乳動物細胞抗體藥物生產上, 積累了豐富的項目開發經驗和管理智慧。

李文捷,美國匹茲堡大學有機化學博士、碩士,北京大學學士,入選江蘇省雙創人才,成都市實體經濟新經濟領域人才,以及南京市紫金山英才先鋒計劃。在近三十載的生物醫藥研發管理中,李文捷博士深耕藥物開發、CMC及CRO/CDMO管理領域,積累了豐富的經驗與深厚的底蘊。他熟悉新藥及仿制藥的工藝研發、生產轉移、工藝驗證、商業化生產及申報等各個環節,能夠精準把控藥物研發的各個流程。此外,李博士還以卓越的學術造詣,在國際期刊上發表學術論文二十余篇,并榮獲近二十項發明專利授權,為行業發展貢獻了寶貴智慧。
AACR年會是癌癥研究領域的全球性盛會,大會邀請了來自世界各地的癌癥科學家,共同分享和討論腫瘤領域的最新科學和醫學研究成果。AACR 以其科學的廣度和卓越的聲譽吸引著該領域的研究人員,促進癌癥研究領域科學家之間新知識新思想的交流與碰撞,提高公眾對癌癥的認識!AACR 不僅包含新靶點的研究進展,也會披露新型的藥物開發。AACR2024 已經公開了多項Late-Breaking Research(突破性研究)。包括Late-Breaking Minisymposium、Late-Breaking Poster Sessions等,將展示在腫瘤基礎研究中的最新發現和腫瘤治療領域中最具有創新價值的療法。下面跟隨美迪西的腳步來看看AACR2024有哪些新機遇?
盡管各種新技術不斷涌現,但小分子依然占半壁江山,新機制療法也持續不斷創新高。KRAS、STAT3、FGFR、STING等“黑馬”小分子領域依舊火熱。

AACR2024會議上KRAS相關的Poster(來自AACR官網)
KRAS是激活一系列信號分子的上游信號傳感器之一,能夠轉導信號從細胞表面傳遞到細胞核,并調控一系列基本的細胞過程,如細胞分化、生長、趨化和凋亡。在KRAS研究項目計劃的制定中,美迪西與客戶進行了深入的溝通。科研骨干結合每個案例的特點,結合多年的實踐經驗和技術積累,向客戶提交了高質量的實驗方案和數據結果。美迪西可提供KRAS靶向藥物發現、CMC研究(API+制劑)、藥效學研究、PK研究、安全性評價等服務。
2022年5月,NMPA批準了信諾維抗腫瘤1類新藥XNW14010的臨床申請,擬用于治療伴有KRAS G12C突變的晚期實體瘤。XNW14010是一種高選擇性的小分子KRASG12C蛋白共價結合抑制劑。臨床前實驗數據顯示XNW14010在不同的腫瘤模型中均有良好的抗腫瘤活性,且呈現良好的量效關系,并具有良好的經口給藥藥代動力學特征和較為理想的安全窗口。
美迪西作為信諾維的合作伙伴,為XNW14010的研發提供了(包括藥代和安全性評價在內)綜合性臨床前研究服務,為項目獲批臨床提供了有力支撐。

AACR2024會議上STAT3相關的Poster(來自AACR官網)
STAT3是一種在多種組織中表達的信號分子,調控一系列與癌細胞生長、增殖、血管生成、轉移、耐藥性和免疫逃逸等有關的基因。STAT3在抑制關鍵的免疫激活調節因子的表達和促進免疫抑制因子的產生方面發揮著重要作用。因此,靶向STAT3信號通路已成為許多癌癥的潛在治療策略。美迪西可以為客戶提供STAT3藥物發現、藥學研究(原料藥工藝開發+制劑)、臨床前研究服務(包括藥效、藥代、安評)以及IND申報等一站式服務。
2023年7月,宇耀生物自主研發的STAT3雙功能磷酸化位點靶向抑制劑——YY201臨床試驗申請正式獲得NMPA批準,適應癥為晚期實體瘤和復發難治性惡性血液腫瘤。宇耀生物科學家團隊一直專注于STAT3靶點的基礎和轉化研究,并借助AI技術首次發現并開發出了納摩爾級STAT3雙磷酸化位點抑制劑、全球領先的First-in-class小分子靶向藥物“YY201”。該藥物通過與STAT3直接結合,抑制STAT3的 Tyr705和Ser727雙位點磷酸化,抑制STAT3功能和阻斷下游信號傳遞,從而發揮抑制腫瘤作用。體外藥理學和藥效學研究表明,YY201與STAT3的親和活性在1-10 nM,在胰腺癌、三陰性乳腺癌、肺癌、急性髓系白血病、淋巴瘤等實體腫瘤和血液腫瘤的體外增殖抑制活性在1-10 nM,在多種體內模型中表現出顯著的抗腫瘤作用,極低劑量下可致腫瘤完全消退,藥代動力學和毒理學研究亦證實YY201良好的成藥性和安全性。
美迪西作為宇耀生物的合作伙伴,為YY201提供了藥學研究服務(包括原料藥、制劑)、臨床前研究服務(包括藥效、藥代、安評)以及IND申報服務等,助力YY201成功通過IND 審批進入臨床試驗階段。
蛋白-蛋白相互作用 (PPI)對于許多細胞過程至關重要。如果發生蛋白質相互作用失調常常會導致多種疾病的發生,如腫瘤和阿爾茨海默病等。所以在蛋白相互作用失調并導致疾病發生時,開發調節這些蛋白相互作用的藥物成了臨床待解決的目標。美迪西針對靶向蛋白降解(TPD)系列(如PROTAC 、分子膠等)藥物研發服務平臺包含設計合成 、進行體外篩選、進行動物體內藥效檢測和 PK/PD 研究、藥學分析、藥物代謝動力學研究和安全性評價,并匯總實驗結果和材料進行IND申報,以助力客戶加快靶向蛋白降解系列藥物藥物的研發進程。美迪西依托20年積累形成的技術優勢和研發平臺優勢,圍繞新藥研發需求不斷拓展產業鏈上下游領域,成功打造了全方位一體化的臨床前CRO服務模式,不僅可將傳統研發環節無縫銜接地串聯,還可整合成并聯式的研發模式,呈現出嚴密計劃、高效協同、有序推進的服務優勢,可更多、更快、更好、更省地賦能新藥研發。

AACR2024會議上PROTAC相關的Poster(來自AACR官網)

AACR2024會議上PROTAC相關的Poster(來自AACR官網)
到目前為止PROTAC仍是生物醫藥領域的熱門研究方向之一。研究和產業化熱潮仍將持續。PROTAC是雙功能小分子,對 E3 泛素連接酶和靶蛋白具有選擇性,并促進靶蛋白的降解。隨著一些基于 PROTAC 的候選藥物進入臨床試驗階段,TPD領域已進入一個新階段,重點充分利用蛋白水解機制來消除致病蛋白。早期工作主要集中在探索新的蛋白靶點以及新的E3連接酶。
2022年8月,睿躍生物(Cullgen)宣布用于治療晚期實體瘤的TRK降解劑(CG001419)新藥臨床研究(IND)申請獲批。CG001419是全球首創(First in class)的TRK (神經營養因子受體酪氨酸激酶)蛋白降解劑。CG001419作為全球首創的高選擇性強效口服靶向蛋白降解劑,其適應癥為用于治療治療NTRK基因融合、NTRK基因點突變和NTRK基因擴增或過表達晚期或轉移性成人實體瘤。作為睿躍生物的合作伙伴,美迪西為CG001419的研發提供了符合中、美GLP規范的(包括藥物代謝動力學研究和安全性評價在內的)綜合性臨床前研究服務,以合規、高效、高質的服務助力其成功獲批。

AACR2024會議上分子膠相關的Poster(來自AACR官網)
分子膠降解劑是一類可誘導E3泛素連接酶底物受體與靶蛋白之間發生相互作用,經泛素化被蛋白酶體降解的小分子。分子膠可以增強和穩定蛋白質相互作用;還能修復因突變而減弱的蛋白質相互作用;且誘導 E3 泛素連接酶與蛋白質靶標的相互作用,進而觸發了靶蛋白的多聚泛素化,通過蛋白酶體降解;分子膠還可以調節蛋白質功能,例如PKM2 是一種與癌癥相關的丙酮酸激酶,在同二聚體形式中活性較低,分子膠可以穩定二聚體并將兩個二聚體“粘合”在一起形成 PKM2 同四聚體,從而增加酶活性。
2023年10月,標新生物第二個分子膠降解劑管線1類新藥GT929膠囊獲得FDA批準進入臨床試驗,用于治療惡性血液腫瘤。該管線此前已于2023年7月獲得NMPA批準開展臨床試驗。GT929是一款靶向IKZF1/3靶點的分子膠,在彌漫大b細胞淋巴瘤動物模型中顯示了極佳的效果。作為標新生物的戰略合作伙伴,美迪西為GT929的研發提供了制劑研究、臨床前研究(包括藥效、藥代、安評)以及撰寫中英文申報資料等服務,為GT929快速實現中美雙報雙批提供了技術保障!
2023年5月,標新生物分子膠降解劑管線1類新藥GT919膠囊獲得FDA批準進入臨床試驗,用于惡性血液腫瘤的治療。該管線此前已于2022年12月20日獲得國家藥品監督管理局(NMPA)批準開展臨床試驗,目前正在中國進行I期臨床研究。對于GT919的研發,美迪西憑借扎實的研發實力,高效完成了其從藥物發現到臨床申報,包括藥物發現、藥學研究、臨床前研究等一站式臨床前研究服務。
近年來偶聯藥物領域可謂是百花齊放,多種新興偶聯藥物的開發取得重要進步,如抗體降解劑偶聯物(AnDC)、病毒樣藥物偶聯物 (VDC)、肽偶聯藥物 (PDC)、小分子偶聯藥物 (SMDC)、抗體細胞偶聯物 (ACC) 以及抗體寡核苷酸偶聯物 (AOC) 等。

AACR2024會議上ADC相關的Poster(來自AACR官網)

AACR2024會議上ADC相關的Poster(來自AACR官網)
ADC是包含抗體、Linker 和細胞毒性有效載荷的生物大分子。目前,正在開發用于腫瘤適應癥的ADC的數量迅速增加,這些ADC藥物給患者、研究人員和藥物開發人員不斷帶來新的機遇和挑戰。美迪西在ADC的臨床前一體化研究方案制定中與客戶深入交流,科研骨干將每一個案例的特點與多年實戰經驗和技術積累相結合,謹慎地將優質實驗方案與結果提交到客戶手上。美迪西可以為客戶提供ADC Payloads合成、ADC藥物偶聯、ADC藥效學評價、ADC藥代動力學評價和ADC安全性評價等服務。截至目前,美迪西承接的IND申報類生物藥大項目已經100多項,包括單抗、雙抗、多抗、ADC、病毒疫苗和融合蛋白等。截至2023年末,美迪西已成功助力23個ADC藥物獲批臨床,并有20+ADC項目在研。
2023年3月,軒竹生物及其旗下全資子公司軒竹康明生物KM501獲得臨床試驗批件。KM501是全球首個完全敲除巖藻糖的雙抗ADC藥物,適用于治療HER2陽性/表達、擴增或突變的局部晚期/轉移性實體瘤,包括HER2低表達的相關晚期腫瘤。KM501為靶向HER2兩個不同結構域雙特異性抗體ADC偶聯物。
美迪西作為軒竹生物的合作伙伴,為KM501提供了符合GLP規范的臨床前研究服務,包括藥代動力學研究和安全性評價。
2023年11月,華奧泰收到美國FDA通知,同意公司研發的靶向CD73抗原的第三代ADC項目HB0052進入臨床試驗,這是華奧泰生物首款獲得FDA批準進入臨床的ADC項目。HB0052是基于華奧泰抗體偶聯藥物平臺研發的首款以拓撲異構酶抑制劑為載荷的First-in-Class創新型免疫抑制靶點的ADC,具有雙重抗腫瘤機制,在多個實體瘤適應癥具有應用潛力。
作為華奧泰的合作伙伴,美迪西依托抗體藥物偶聯物研發服務平臺及其專業的技術能力和豐富的項目經驗,為HB0052的研發提供了符合GLP規范的藥代、安評試驗,保障項目高質高效推進。
2024年2月,國藥集團中國生物上海生物制品研究所自主研發的第二款I類創新型ADC藥物 SIBP-A17獲得國家藥品監督管理局臨床試驗批準通知書。該產品擬用于在晚期惡性實體瘤患者中開展臨床試驗。
美迪西作為上海生物制品研究所的合作伙伴,為SIBP-A17的研發提供了藥代動力學和安全性評價等臨床前研究服務。這是美迪西在ADC領域助力研發成果快速落地的又一個成功案例。
近年來,抗體類藥物(如單抗、雙抗、ADC等)發展迅速,在多個疾病研究領域均有重磅產品陸續上市,抗體藥物研發受到越來越多的關注。

AACR2024會議上抗體相關的Poster(來自AACR官網)
美迪西在抗體藥物的一站式研發服務方案制定中與客戶深入交流,將每一個案例的特點與多年實戰經驗和技術積累相結合,謹慎地將優質實驗方案與結果交到客戶手上。美迪西可以提供抗體全流程服務,包括:藥物發現、CMC研究服務、符合GLP規范的綜合性臨床前研究服務(藥效學研究、藥代動力學評價和安全性評價等);以合規、高效、高質的服務助力客戶產品順利獲批等。美迪西抗體藥物研發服務平臺建立至今已積累了眾多國內外知名醫藥企業及科研機構客戶,已成功助力濟民可信、百奧泰、石藥集團等藥企的抗體項目獲批臨床,并達成多年的持續合作,獲得客戶持續的信任和好評。截至2023年末,美迪西已成功助力32個抗體藥物獲批臨床,另外有多個抗體項目在研。
2022年10月,HCW Biologics Inc.融合蛋白復合物HCW9218獲FDA批準進行癌癥治療試驗。HCW9218是一種異源二聚體、雙功能融合蛋白復合物,包含TGF-β受體II的細胞外結構域和IL-15/IL-15受體α復合物,能有效激活和增殖NK細胞和CD8+ T細胞,增強細胞對腫瘤靶標的細胞毒性,優化化療的療效并減少化療副作用。
美迪西作為HCW的合作伙伴,在GLP的實驗室環境和操作規范下,建立了適用于HCW9218的分析方法,提供了臨床前藥代和安評研究,全力促成該項目的高質高效完成。此外,美迪西臨床前藥理及毒理研究團隊依托在軟件、技術、規范、素質等各方面全面成熟的SEND數據轉換平臺,助力HCW9218成功申報FDA,推動其進入臨床試驗階段。
2023年7月,邏晟生物NB002順利通過FDA審查并同意開展Ⅰ期臨床試驗。NB002是一款靶向TIM-3獨特表位的單克隆治療抗體,具有顯著的單藥抗腫瘤的治療效果,其不僅顯著激活T和NK細胞的活性,增強其對抗腫瘤的能力,更重要的是NB002重建了腫瘤環境中被抑制的天然免疫,恢復DC細胞反應能力,提高髓系細胞抗原遞呈功能,整體性解除TIM-3調控的從天然免疫到獲得免疫的抑制性作用,有效地增強腫瘤免疫殺傷能力。
美迪西作為邏晟生物的合作伙伴,為NB002提供了安全性評價、藥代動力學等臨床前研究服務,助力其IND申請順利獲FDA臨床許可。
除了上述Late-Breaking Research(突破性研究),美迪西還將持續關注2024 AACR更多研究進展。若您還想了解更多有價值的新技術或者服務,請發送郵件至marketing@medicilon.com.cn,歡迎隨時咨詢!同時美迪西美國團隊將出席此次AACR會議,展位號是 4021。歡迎現場交流!

 相關新聞
相關新聞